Рассмотрим образование некоторых комплексов с позиций ТВС. Например, катион [Zn(NH3)4]2+ включает комплексообразователь цинк(II). Электронная оболочка этого условного иона имеет формулу[Ar] 3d10 4s0 4p0 и может быть условно изображена так: Вакантные 4s- и 4p-орбитали атома цинка(II) образуют четыре sp3-гибридные орбитали, ориентированные к вершинам тетраэдра. Каждая молекула аммиака имеет неподеленную пару электронов у атома азота. Орбитали атомов азота, содержащие неподеленные пары электронов, перекрываются с sp3-гибридными орбиталями цинка(II), образуя тетраэдрический комплексный катион тетраамминцинка(II) [Zn(NH3)4]2+: Поскольку в ионе [Zn(NH3)4]2+ нет неспаренных электронов, то он проявляет диамагнитные свойства.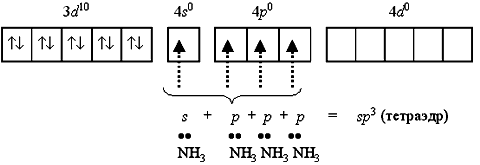
тетракарбонилникель [Ni(CO)4]. Напишем электронную формулу валентного уровня комплексообразователя. Например, для нейтрального атома никеля: Переход 4s-электронов на 3d-подуровень превращает парамагнитный атом Ni0 в диамагнитную частицу Ni* Полученные вакантные орбитали подвергаются гибридизации, образуя тетраэдрическую конфигурацию.

