Закон Бойля Мариотта устанавливает зависимость между удельным объёмом идеального газа и его давлением при постоянной температуре.
Т = const, PV= const
Для данной массы газа при постоянной температуре произведение давления на объём есть величина постоянная.
Т.е. давление изменяется обратно пропорционально изменению объёма и при этом выполняется соотношение:
P1V1 = P2V2,
где P1 и V1 – начальные параметры газа, P2 и V2 – конечные параметры газа.
Закон Гей-Люссакаустанавливает зависимость объёма идеального газа от его температуры при постоянном давлении.
P = const, 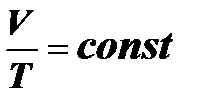
Для данной массы газа при постоянном давлении объём идеального газа изменяется прямо пропорционально изменению абсолютной температуры.
Объём изменяется прямо пропорционально изменению абсолютной температуры.
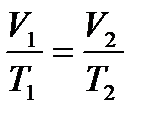
где Т1 и V1 – начальные параметры газа, Т2 и V2 – конечные параметры газа.
Закон Авагадро устанавливает, что при одинаковых физических условиях в различных газах содержится одинаковое число молекул. Экспериментально было найдено, что числоАвагодро численно равно 6.022045·1023 моль-1.
Из закона Авагодро вытекает важное следствие.
При одинаковых физических условиях произведение удельного объёма газа на его молярную массу есть величина постоянная.
Закон Менделеева-Клапейрона. Это уравнение однозначно связывает между собой параметры газа P, v, Т. Уравнение впервые было получено Клапейроном в 1884 г. и названо его именем.
Для произвольного количества идеального газа уравнение состояния имеет вид
PV = mRT ,
где Р – абсолютное давление, Па; V – объём газа, м3; m – масса газа, кг; Т – абсолютная температура, К; R - постоянная величина, не зависящая от состояния газа и является индивидуальной для каждого газа. Эту величину, отнесённую к 1 кг газа, называют удельной газовой постоянной.

