Постулати Бора
Формулювання[ред. • ред. код]
1. Атомна система може перебувати тільки в особливих стаціонарних, або квантових станах, кожному з яких відповідає певна енергія  . У стаціонарному стані атом енергію не випромінює.
. У стаціонарному стані атом енергію не випромінює.
2. У стаціонарному стані атома електрон повинен мати дискретні (квантовані) значення моменту імпульсу. Радіуси 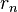 орбіт електронів задовольняють умову:
орбіт електронів задовольняють умову:
 ,
,
де  - маса електрона,
- маса електрона, 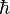 - зведена стала Планка.
- зведена стала Планка.
3. Перехід атома з одного стаціонарного стану в інший супроводжується випромінюванням чи поглинанням фотонів, енергію яких  визначають за формулою:
визначають за формулою:
 ,
,
де 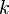 і
і  - цілі числа (номери стаціонарних станів), якщо
- цілі числа (номери стаціонарних станів), якщо 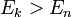 фотон з частотою
фотон з частотою  випромінюється, якщо
випромінюється, якщо  - поглинається.
- поглинається.
Поглинаючи світло, атом переходить із стаціонарного стану з меншою енергією в стаціонарний стан з більшою енергією. Усі стаціонарні стани, крім одного, є умовно стаціонарними. Нескінченно довго кожен атом може знаходитись лише в стаціонарному стані з мінімальним запасом енергії. Цей стан атома називається основним, всі інші - збудженими.
Спектроскопія[ред. • ред. код]
Спектроскопíя — розділ фізики, присвячений вивченню спектрів електромагнітного випромінювання. Слово "спектроскопія" походить від латинського слова "spectrum" (привид) і грецького "skopos" (спостерігач).
Загальний опис[ред. • ред. код]
Дані спектроскопії – найважливіша основа для вивчення будови атомів та молекул, речовини в її різних аґреґатних станах, зокрема різноманітних мінералів. На С. базується спектральний аналіз. Див. також інфрачервона спектроскопія.
Спектроскопія забезпечує отримання інформації про атоми, молекули, йони, кристали і може використовуватися для визначення структури і складу зразка. Спектроскопія - неоцінимий аналітичний метод, що реалізовується на різних типах спектрометрів (або спектрофотометрів) - ЯМР, ІЧ, УФ, видимої і ближньої ІЧ частини спектра, флуоресцентних спектрометрах.
Аналіз спектрів дозволяє визначати енергетичні рівні досліджуваної системи. Також з наявності й інтенсивності випромінювання певного роду в спектрах проводять якісний і кількісний аналіз складу речовини.
Можна виділити два типи спектроскопії. У рамках класичної спектроскопії спектр отримують завдяки розкладу світла призмою, або дифракційною ґраткою.
Другий тип — Фур'є спектроскопія. У цьому випадку вимірюється часова залежність коливання системи. Після виконання перетворення Фур'є отримують частотну характеристику системи.
Спектроскопія відбиття – вивчає спектри відбиття електромагнітного випромінювання речовин у видимій, УФ та ІЧ-областях. Для реєстрації спектрів відбиття використовуються спетрофотометри. С.в. застосовуються для вивчення складу і будови поверхневих шарів твердих тіл та мутних середовищ, а також для ідентифікації адсорбованих хімічних сполук.




