СИСТЕМА ГЕМОСТАЗА
Термином «гемостаз» обозначают все процессы, направленные на сохранение крови в сосудистом русле, предотвращение кровоточивости и восстановление кровотока при окклюзии (закупорке) сосуда тромбом.
Нормальное состояние крови, необходимое для поддержания адекватного кровообращения, обеспечивается динамическим равновесием между тремя основными системами:
- свертывающей;
- противосвертывающей;
- фибринолитической.
Гемостаз осуществляется путем взаимодействия между тремя основными компонентами:
- стенкой кровеносных сосудов;
- клетками крови (в первую очередь - тромбоцитами);
- плазменными ферментными системами (свертывающей, фибринолитической, калликреин-кининовой).
Свертывающая система крови
Эндотелий сосудов. Кровь циркулирует в организме, оставаясь в жидком состоянии только до момента соприкосновения с эндотелием. Этот внутренний слой кровеносных сосудов обладает уникальным строением клеточных мембран, препятствующих свертыванию крови. Кроме того, эндотелий продуцирует ряд активных веществ, обладающих противосвертывающими свойствами и вызывающих дилатацию сосудов - простациклин I2, оксид азота (NO).
При повреждении эндотелия сосудов кровь вступает в контакт с белками субэндотелиального слоя - коллагеновыми и эластиновы-ми волокнами, фибробластами, мышечными клетками и базальной мембраной сосуда. Кроме того, в субэндотелиальном слое накапливается стимулятор адгезии тромбоцитов - фактор Виллебранда.
Тромбоцитарный (первичный) гемостаз. Первыми на повреждение эндотелия реагируют тромбоциты. Фактор Виллебранда, находящийся в субэндотелиальном слое, соединяется с рецепторами на поверхности тромбоцитов, что обеспечивает их адгезию (прикрепление) к субэндотелию. Агрегация тромбоцитов происходит локально (в месте повреждения эндотелия), а в других участках сосуда сохранный эндотелий препятствует процессу тромбообра-зования.
Плазменный гемостаз. Одновременно с тромбоцитами активизируются плазменные факторы свертывания. Скорость активации конечного звена гемостаза (плазменного) зависит от объема поражения, при повреждении крупных сосудов этот процесс завершается быстрее (рис. 26-1).
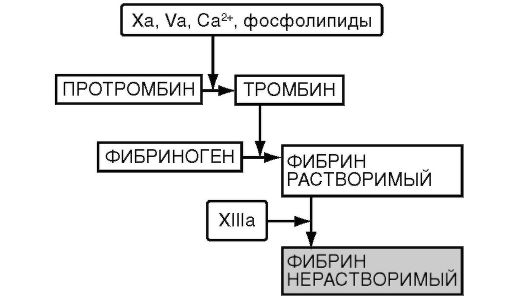
Рис. 26-1. Конечный этап свертывания крови (схема)
Противосвертывающая система крови ограничивает процесс свертывания непосредственно на участке повреждения сосуда, предотвращая неограниченное тромбообразование. Первый компонент этой системы - фактор свертывания X, который в комплексе с липопро-теинсвязанным ингибитором инактивирует фактор VII, тем самым блокируя внешний путь свертывания.
Протеазы внутреннего пути свертывания (факторы XII, XI, X и IX) блокирует антитромбин III (кофактор гепарина). Факторы VIII и V блокируются протеином С (кофактор - протеин S). Оба эти белка синтезируются в печени при участии витамина К. Наконец, на поверхности эндотелия содержится белок тромбомодулин, который обладает способностью инактивировать тромбин.
Фибринолитическая система расщепляет фибрин, восстанавливая проходимость сосудов. Основной компонент этой системы - плаз-мин - образуется из неактивного предшественника плазминогена под воздействием факторов, образующихся в клетках эндотелия (тканевый активатор плазминогена и урокиназа). Плазмин расщепляет фибрин на отдельные мелкие фрагменты - так называемые продукты деградации фибрина. Активность фибринолиза регулируется системой ингибиторов, важнейшими из которых считают ингибитор тканевого активатора плазминогена и а1-антиплазмин.
26.2. ТРОМБОФИЛИИ
Тромбофилии - наследственные или приобретенные изменения в системе гемостаза, создающие высокий риск развития и рецидивиро-вания тромбозов и тромбоэмболий, приводящих к ишемии и инфарктам внутренних органов (миокарда, мозга, почки, селезенки). Повышенная опасность тромбообразования отмечается при следующих состояниях.
• Атеросклероз коронарных артерий. Образование тромба в коронарных артериях - единственная причина ИМ и нестабильной стенокардии. Причиной тромбозов в данном случае можно считать разрыв атеросклеротических бляшек1. Расширение камер сердца (при сердечной недостаточности) предрасполагает к образованию пристеночных тромбов. Другой причиной тромбозов камер сердца может стать длительно существующее нарушение сердечного ритма, состояние после оперативных вмешательств на сердце и имплантации искусственных клапанов.
• Болезни вен.
• Гиподинамия (у лежачих больных), иммобилизация конечностей и туловища или снижение скорости периферического кровотока (у больных сердечной недостаточностью).
• Злокачественные новообразования с распадом опухоли и выделением в кровь большого количества тканевого тромбопластина.
• Сепсис у больных тяжелыми инфекциями.
• Аутоиммунные заболевания (антифосфолипидный синдром).
• Внезапная отмена прямых антикоагулянтов.
1 Отложение в субэндотелиальном слое ХС, липидов и кальция. При повреждении эндотелия контакт крови с компонентами бляшки инициируют развитие тромбов (подробно см. главу «Инфаркт миокарда»).
Симптомы тромбозов и тромбоэмболий
Как следует из указанного выше, тромбофилия не является заболеванием и представляет собой звено патогенеза многих болезней человека. Симптомы тромбозов очень разнообразны и определяются тем, в каких именно органах они происходят. Можно выделить несколько наиболее частых симптомов.
• Тромбозы коронарных артерий (нестабильная стенокардия, острый ИМ - см. гл. 11) сопровождаются болями, нарушением сердечного ритма и проводимости, развитием сердечной недостаточности и могут привести к смерти больного.
• Тромбозы и тромбоэмболия легочных артерий (ТЭЛА) сопровождаются внезапным появлением одышки, потерей сознания, аритмиями и могут привести к смерти больного.
• Тромбозы и тромбоэмболии артерий головного мозга (ОНМК, см. приложения) сопровождаются разнообразными неврологическими нарушениями.
• Тромбозы вен нижних конечностей часто возникают на фоне варикозной болезни, у больных гиподинамией, иммобилизацией конечностей после хирургических операций, у лиц с сердечной недостаточностью. Для тромбоза вен нижних конечностей характерны боли, отек и припухлость, а при сопутствующей инфекции возникает локальная гиперемия1и повышается местная температура. Тромбы в нижних конечностях могут отрываться и мигрировать вместе с током крови, приводя к развитию ТЭЛА.
Диагноз и методы обследования
На практике иногда бывает трудно различить тромбоз и другое заболевание сосудов - атеросклероз. Однако при атеросклерозе проходимость сосудов нарушается постепенно и симптомы недостаточного кровоснабжения органов прогрессируют достаточно долго. При тромбозе или тромбоэмболии эти симптомы развиваются внезапно и быстро.
Для уточнения диагноза тромбоза крупных вен и артерий применяют ультразвуковое сканирование и ультразвуковую допплеро-графию2. Нарушение кровоснабжения сердца, почек и головного мозга можно диагностировать на основании данных ангиографии3.
1 Гиперемия - покраснение, связанное с избытком крови, отток которой нарушен.
2 Метод, позволяющий определить скорость кровотока в отдельном участке сосуда.
3 Рентгеновский метод исследования, перед его проведением исследуемый сосуд заполняют рентгеноконтрастным веществом.
Однако обычно диагноз устанавливают, основываясь на вторичных признаках, свидетельствующих о гибели тканей. Например, повышение в крови активности МВ-фракции креатининфосфокиназы свидетельствует о гибели клеток миокарда при инфаркте, а внезапный паралич конечностей - об инсульте.
Большое значение для диагностики и лечения тромбозов имеет исследование состояния гемостаза путем анализа свертывающей системы крови. Показатели коагулограммы позволяют выявить несколько индикаторов состояния гемостаза и контролировать эффективность и безопасность ЛС, влияющих на гемостаз (табл. 26-1).
Таблица 26-1. Лабораторная оценка показателей гемостаза
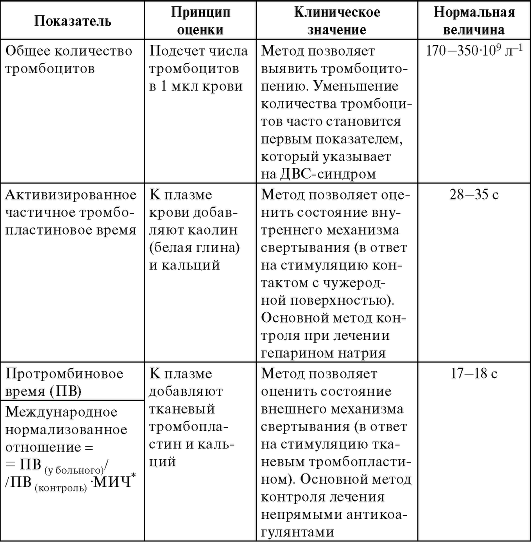
Окончание табл. 26-1

*МИЧ - международный индекс чувствительности тробмопластина: реактива для определения протромбинового времени.
Клинико-фармакологические подходы к лечению тромбозов и профилактике тромбофилии
Выбор ЛС для лечения тромбозов представлен в табл. 26-2. Поскольку в образовании тромбов участвует несколько механизмов, при лечении подобных состояний обычно назначают несколько препаратов с различным действием. Например, при нестабильной стенокардии одновременно применяют дезагреганты и прямые антикоагулянты.
Таблица 26-2. Клинико-фармакологические подходы к назначению дезагре-гантов и антикоагулянтов
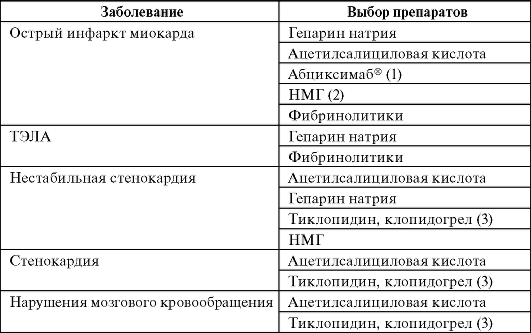
Окончание табл. 26-2
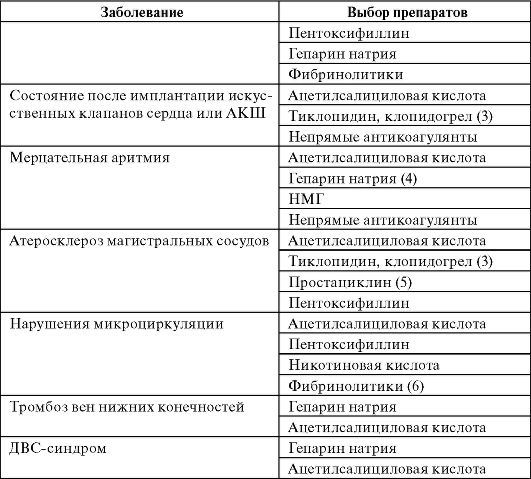
Обозначения: (1) - применяется в дополнение к ацетилсалициловой кислоте и гепарину натрия при проведении ангиопластики и тромболизиса; (2) - при ИМ без зубца Q; (3) - при непереносимости или неэффективности ацетилсалициловой кислоты; (4) - при подготовке к кардиоверсии (восстановленного ритма); (5) - не назначают в раннем периоде после ИМ (сосудорасширяющее действие); (6) - с последующим наложением кава-фильтра.
Из препаратов, влияющих на процессы свертывания, наиболее широко применяют ацетилсалициловую кислоту в малых дозах (75- 375 мг/сут). Ее назначают при поражении коронарных, мозговых и периферических сосудов (стенокардии, острого ИМ, ишемическо-го инсульта, атеросклероза нижних конечностей), для уменьшения вероятности повторных тромбозов и тромбоэмболии, при хирургических вмешательствах (протезировании клапанов сердца).
Тиклопидин и клопидогрел назначают для профилактики и лечения преходящего нарушения мозгового кровообращения у боль-
ных, которые не переносят ацетилсалициловую кислоту (например, при аспириновой БА), или когда эпизоды нарушения мозгового кровообращения рецидивируют, несмотря на прием этого препарата (явление, называемое «аспиринорезистентность»). Кроме того, эти ЛС применяют для профилактики острого ИМ, лечения заболеваний сосудов, возникающих на фоне СД (см. гл. 17), при хронических облитерирующих заболеваниях артерий, для профилактики тромбозов сосудистых протезов, при гемодиализе (см. табл. 26-2).
Из-за более частых побочных эффектов тиклопидина и его более высокой стоимости, по сравнению с ацетилсалициловой кислотой, это ЛС считают препаратом второго ряда для лечения больных нестабильной стенокардией и нарушением мозгового кровообращения и назначают при наличии противопоказаний к ацетилсалициловой кислоте или ее неэффективности.
Антагонисты гликопротеиновых рецепторов тромбоцитов GP IIb/IIIa назначают (в дополнение к ацетилсалициловой кислоте и гепарину натрия) при коронарной ангиопластике у больных нестабильной стенокардией или острым ИМ.
Для лечения функциональных и органических ишемических нарушений кровообращения в конечностях (болезнь Рейно, обли-терирующий эндартериит, атеросклероз, диабетическая ангиопатия) обычно назначают пентоксифиллин. Его применение эффективно также при трофических язвах, посттромбофлебитическом синдроме, лечении и профилактике некоторых форм тромбозов и эмболий (в сочетании с другими препаратами).
Гепарин натрия применяют для профилактики и лечения тромбозов, тромбоэмболий различной локализации - как венозных, так и артериальных. Препарат назначают при ТЭЛА, нестабильной стенокардии и остром ИМ, тромбозе глубоких вен нижних конечностей, балонной ангиопластике и протезировании клапанов сердца, нарушениях мозгового кровообращения, ДВС-синдроме, тромбоэмболи-ческих заболеваниях у беременных (см. табл. 26-2).
Кроме того, гепарин натрия назначают в составе комплексной терапии и для профилактики не только тромбозов, но и многих заболеваний сосудов - микротромбозоваскулитов, гломерулонефрита и др.
В настоящее время широко применяют низкомолекулярные гепа-рины (отличаются меньшей частотой НЛР и не требуют мониторинга
АЧТВ).
Непрямые антикоагулянты (аценокумарол, варфарин, фениндион) применяют для поддержания гипокоагуляции в течение длительного
времени - многих месяцев и даже лет, или когда гепарины недостаточно эффективны (например, при дефиците или аномалиях антитромбина III). Непрямые антикоагулянты назначают больным с имплантированными искусственными клапанами сердца, при угрозе тромбоэмболий, МА и повторном проведении кардиоверсии, рецидивирующих сосудистых тромбозах, тромбозе глубоких вен голеней. При непереносимости кумариновых антикоагулянтов назначают фениндион.
Показаниями к проведению тромболитической терапии считают тромбозы коронарных артерий сердца и острые инфаркты миокарда с подъемом сегмента ST и патологическим зубцом Q на ЭКГ, ТЭЛА, тромбоз вен (с наложением кава-фильтра), тромбоэмболический ишемический инсульт.
Контроль эффективности и безопасности лечения
Основная опасность применения дезагрегантов, антикоагулянтов и фибринолитиков - риск возникновения кровотечений. Для проведения безопасного и эффективного лечения используют клинические (по характеру жалоб и данным осмотра больного) и лабораторные индикаторы - табл. 26-3.
Таблица 26-3. Оценка эффективности и безопасности при назначении деза-грегантов и антикоагулянтов

Окончание табл. 26-3

26.3. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ
ДЕЗАГРЕГАНТОВ
Дезагреганты влияют на тромбоцитарное звено гемостаза путем угнетения агрегации тромбоцитов. Это способствует «остановке» роста тромбов и предотвращает образование новых. По механизму действия дезагреганты разделяют на четыре группы:
- ингибиторы циклооксигеназы 1: ацетилсалициловая кислота;
- блокаторы рецепторов к аденозиндифосфата типа P2Y12: тикло-пидин и клопидогрел;
- блокаторы гликопротеиновых IIB/IIIA рецепторов: абцикси-маб , тирофибан , эптифибатид;
- ингибиторы фосфодиэстеразы.
Ингибиторы циклооксигеназы 1. Ацетилсалициловая кислота - наиболее часто применяемый при лечении и профилактике сердечно-сосудистых заболеваний дезагрегант. Механизм действия ацетилсалициловой кислоты заключается в торможении агрегации тромбоцитов путем необратимого подавления активности цикло-оксигеназы 1, что приводит к уменьшению синтеза тромбоксана А2 (рис. 26-2). Необратимым торможением тромбоцитарной цикло-оксигеназы 1 объясняется тот факт, что антиагрегантный эффект ацетилсалициловой кислоты сохраняется в течение 5-7 сут после однократного его приема. Антиагрегантный эффект ацетилсалициловой кислоты реализуется при назначении в дозе 75-375 мг/сут; при ее увеличении возможен даже проагрегантный эффект, обусловленный подавлением образования простациклина в эндотелии сосудов.
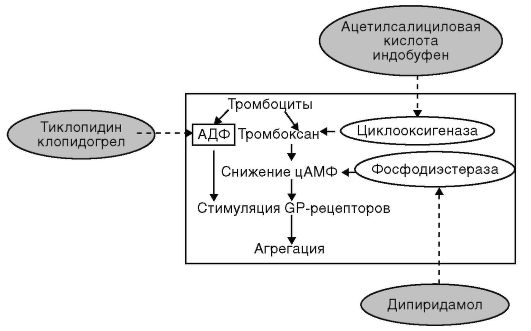
Рис. 26-2. Точки приложения действия антитромбоцитарных препаратов
Ацетилсалициловая кислота быстро и полностью всасывается при приеме внутрь, максимальная концентрация в крови достигается через 20-30 мин. Препарат подвергается биотрансформации путем гидролиза с участием карбоксиэстераз при «первом прохождении» через печень с образованием активных метаболитов (салициловой кислоты), которые выводятся в основном почками.
Ацетилсалициловую кислоту принимают внутрь, в том числе в виде специально разработанных кишечнорастворимых лекарственных форм (Тромбо АСС*, Аспирин-кардио*), что позволяет избежать контакта ЛС со слизистой оболочкой желудка и снизить риск ее поражения. Для быстрого достижения антиагрегантного эффекта назначают ацетилсалицилат лизина®, который вводят парентерально (внутримышечно, внутривенно струйно или капельно).
Блокаторы рецепторов к аденозиндифосфата типа P2Y12. К блока-торам рецепторов к аденозиндифосфата типа P2Y12 или производным тиенопиридина относят клопидогрел (плавикс*, зилт*) и тиклопидин (тиклид*). Они проявляют свои антитромбоцитарные свойства путем подавления агрегации тромбоцитов, индуцируемой аденозиндифос-фатом. В основе механизма действия препаратов лежит необратимая блокада рецепторов к аденозиндифосфата типа P2Y12 на мембране тромбоцитов. Антиагрегантный эффект клопидогрела и тиклопи-
дина несколько выше по сравнению с ацетилсалициловой кислотой. Антиагрегантный эффект проявляется через 2 ч после приема кло-пидогрела и несколько позже после приема тиклопидина - через 24-48 ч. Стабильный антиагрегантный эффект развивается на 3-7-е сутки приема препаратов.
Клопидогрел и тиклопидин принимают внутрь. Эти препараты хорошо всасываются (биодоступность составляет 80-98%). Тиклопидин представляет собой активное соединение и подвергается биотрансформации в печени под влиянием CYP2C19 с образованием активного метаболита. Клопидогрел, в отличие от тиклопидина, - пролекарство: в печени под влиянием CYP2C19 и CYP3A4 образуется активный метаболит (4-оксаклопидогрел). Препараты выводятся почками в виде метаболитов.
Блокаторы гликопротеиновых ПБ/ШЛ рецепторов. Для данной группы препаратов характерно торможение конечного этапа агрегации тромбоцитов, а именно процесса построения тромбоцитарного тромба посредством образования мостиков между соседними активированными тромбоцитами. Препараты блокируют участок взаимодействия активированных гликопротеинов IIb/IIIa на поверхности тромбоцитов с фибриногеном и некоторыми другими факторами. В отличие от ацетилсалициловой кислоты, клопидогрела и тиклопидина, анти-агрегантный эффект блокаторов гликопротеиновых IIb/IIIa рецепторов наступает сразу после их внутривенного введения. К препаратам из этой группы относят абциксимаб®, тирофибан*3, эптифибатид. Их применяют только внутривенно (болюсное введение с последующим капельным), в условиях кардиореанимационных отделений у больных нестабильной стенокардией или ИМ, после проведения коронарной ангиопластики (постановки стентов в коронарные артерии). Эти препараты самые дорогие из антиагрегантов.
Ингибиторы фосфодиэстеразы. К препаратам из этой группы относят пентоксифиллин (трентал*, агапурин*) и дипиридамол (куран-тил*). Препараты блокируют фосфодиэстеразу в тромбоцитах, увеличивая в них концентрацию цАМФ, что приводит к торможению агрегации тромбоцитов и эритроцитов, а также увеличивает их деформируемость и улучшает микроциркуляцию крови. Благоприятный эффект пентоксифиллина при нарушении периферического кровообращения в большей степени связан с улучшением микроциркуляции. Пентоксифиллин умеренно усиливает кровоток в почках, что приводит к незначительному увеличению диуреза и натрийуреза. Дипиридамол, кроме того, усиливает коронарный кровоток.
Пентоксифиллин и дипиридамол хорошо всасываются, подвергаются биотрансформации в печени до неактивных метаболитов, которые выводятся почками. Дипиридамол назначают внутрь, пен-токсифиллин принимают внутрь и вводят внутривенно.
НЛР. Все дезагреганты могут вызывать различные кровотечения, в том числе опасные для жизни (желудочно-кишечные, кровоизлияния в мозг). Наиболее часто они возникают при применении блокаторов гликопротеиновых IIb/IIIa рецепторов, реже - ацетилсалициловой кислоты, клопидогрела и тиклопидина. Группами риска развития кровотечений при применении дезагрегантов считают больных язвенной болезнью, с кровотечениями в анамнезе, принимающих другие ЛС, вызывающие кровотечения (антикоагулянты, фибринолитики). Этим категориям пациентов рекомендовано совместное применение дезагрегантов с ингибиторами протонной помпы (омепразол), что снижает риск развития желудочно-кишечных кровотечений. Однако при применении дезагрегантов не требуется контролировать параметры коагулограммы из-за отсутствия достоверных методов оценки активности тромбоцитарного звена гемостаза. Для ацетилсалициловой кислоты характерны реакции со стороны ЖКТ: ульцерогенное действие1 (образование язв, эрозий желудка, двенадцатиперстной кишки), диспепсия. Кроме того, ацетилсалициловая кислота может вызывать бронхоспазм при применении у больных с аспириновым вариантом БА. Для тиклопидина характерно миелотоксическое действие2, которое может проявляться нейропе-нией (снижение количества нейтрофильных гранулоцитов в крови), вплоть до агранулоцитоза (исчезновение нейтрофильных грануло-цитов в крови), что сопровождается иммунодефицитом, а следовательно, и развитием опасных для жизни инфекций. Соответственно при применении тиклопидина необходимо 1 раз проконтролировать общий анализ крови. Дипиридамол и реже пентоксифиллин у пациентов со стенозирующим атеросклерозом коронарных артерий могут вызывать «синдром обкрадывания»3. При внутривенном введении пентоксифиллина характерны чувство прилива к голове, жара в голо-
1 Ульцерогенный - способствующий образованию язвенных дефектов слизистой оболочки ЖКТ.
2 Миелотоксическое действие - токсическое поражение костного мозга, сопровождающееся нарушением кроветворения.
3 «Синдром обкрадывания» - состояние перераспределения кровотока в миокарде: при расширении неповрежденных сосудов испытывают недостаток кровоснабжения участки миокарда, которые снабжаются поврежденными атеросклерозом артериями.
ве и конечностях, что может сопровождаться гиперемией кожи лица и связано с вазодилатирующим действием пентоксифиллина в отношении сосудов кожи.
Противопоказания к применению. Дезагреганты абсолютно противопоказаны при кровотечениях любой локализации. Обострение язвенной болезни считают относительным противопоказанием, и в случаях, когда польза от применения антиагрегантов превышает риск, допустимо назначение этой группы ЛС в сочетании с ингибиторами протонной помпы. Пентоксифиллин и дипиридамол противопоказаны больным острым ИМ и нестабильной стенокардией. Ацетилсалициловая кислота противопоказана при аспириновом варианте БА.
Взаимодействие дезагрегантов с другими препаратами. Риск кровотечений увеличивается при совместном применении дезагреган-тов с антикоагулянтами (гепарином натрия, варфарином, ацено-кумаролом, фениндионом), фибринолитиками. Глюкокортикоиды усиливают ульцерогенное действие ацетилсалициловой кислоты. Препараты, ингибирующие CYP3A4 (противогрибковые ЛС - производные азолов, макролиды), могут снижать антиагрегантное действие клопидогрела. Описано снижение антиагрегантного действия клопидогрела при его соместном применении с ЛС, подвергающимися биотрансформации с участием CYP3A4 (антагонистами кальция) и CYP209 (ингибиторами протонного насоса), при этом возникает конкурентное взаимодействие ЛС за данный изофермент.
26.4. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ АНТИКОАГУЛЯНТОВ ПРЯМОГО ДЕЙСТВИЯ
Антикоагулянтами прямого действия называют такие препараты, которые оказывают непосредственное влияние на активность циркулирующих в крови факторов свертывания. Общим свойством применяемых в настоящее время прямых антикоагулянтов считают их способность тормозить ферментативную активность тромбина (или фактора Па), который имеет большое значение в тромбооб-разовании. Следовательно, по основному механизму антитромбо-тического действия все прямые антикоагулянты можно рассматривать как ингибиторы тромбина. Препараты этой группы, так же как и дезагреганты, останавливают рост тромбов и предотвращают образование новых.
Фармакокинетика. Биодоступность гепарина натрия невысока, на нее влияют множество факторов (взаимодействие с белками плазмы, захват клетками эндотелия и макрофагами, активность тромбоцитов). Препарат не проникает через плаценту и в молоко. Подвергается биотрансформации в печени и почках до низкомолекулярных фрагментов. В неизмененном виде элиминируется почками только при внутривенном введении в больших дозах. Период полувыведения укорочен у курильщиков, резко уменьшен при ТЭЛА и незначительно - при венозных тромбозах, остром некрозе печени, может увеличиваться при выраженных нарушениях функций почек и печени. Низкомолекулярные гепарины выводятся медленнее обычного гепарина натрия и характеризуются более длительным периодом полувыведения, а следовательно, действуют дольше, что обусловливает меньшую кратность применения (1-2 раза в сутки).
Фармакодинамика. Антикоагулянтный эффект гепарина натрия обусловлен связыванием с антитромбином III и образованием комплекса, который в первую очередь инактивирует тромбин (фактор Па). Препарат подавляет также Xa, IXa, VIIa и другие факторы свертывания крови. Ингибирование тромбина сопровождается гипокоа-гуляцией (подавляется переход фибриногена в фибрин и увеличивается АЧТВ). Ингибирование протромбиназы (фактор Ха) в основном проявляется антитромботическим действием. Ингибируя медиаторы воспаления (гистамин, серотонин, калликреин), гепарин натрия оказывает противовоспалительное действие.
Гепарин натрия - естественный прямой антикоагулянт, состоящий из цепей сульфатированных гликозаминогликанов различной длины и молекулярной массы. От длины цепей зависят биологические эффекты гепарина натрия. Различают следующие группы этих цепей:
- фракции, состоящие из ди- и тетрасахаридов, которые лишены сродства к антитромбину III и не обладают антикоагулянтным действием, но оказывают влияние на некоторые другие процессы;
- фракции с молекулярной массой 1700-5400 Да, характеризующиеся высокой способностью в комплексе с антитромбином III инактивировать фактор Ха и в более слабой степени - тромбин; эти фракции составляют основу низкомолекулярных гепаринов;
- крупномолекулярные фракции (молекулярная масса от 5400 до 24 000 Да), обладающие в комплексе с антитромбином III
преимущественно антитромбиновым и антикоагулянтным действиями, но значительно более слабым ингибирующим влиянием на фактор Ха; в большинстве препаратов эти фракции господствуют, благодаря чему эти препараты обладают преимущественным анти-Ха и антикоагулянтным действием.
Гепарин вырабатывается тучными клетками, расположенными во всех тканях организма, наибольшая их концентрация отмечена в легких и печени. Гепарин для клинического применения получают из слизистых оболочек свиньи и легких крупного рогатого скота. Наиболее широко используют натриевую и кальциевую (кальципа-рин®, гепарибене®) соли гепарина. Кальциевые соли гепарина применяют только подкожно. Препараты гепарина различаются по происхождению, степени очистки и содержанию, и их дозы выражают не в миллиграммах, а в единицах (ед).
Оптимальный метод лечебного применения гепарина натрия - длительная внутривенная инфузия, которую при необходимости достижения быстрой гипокоагуляции (острые или массивные тромбоэмболии) можно начинать с предварительного болюсного введения препарата. Необходимую дозу препарата подбирают по показаниям АЧТВ (см. табл. 21-1). При лечении большинства видов тромбозов вводят такие дозы гепарина натрия, которые обеспечивают АЧТВ в 1,5-2,0 раза выше нормы.
С профилактической целью малые дозы гепарина натрия вводят подкожно (в область живота). К внутримышечным введениям гепарина натрия прибегать не следует. Это обусловлено тем, что в богато васкуляризованной мышечной ткани мест инъекций быстро образуются не всегда выявляемые, но легко инфицирующиеся гематомы, из которых препарат все хуже и хуже резорбируется в кровь. С этим связаны непредсказуемые перепады антикоагулянтного действия препарата. Возможно местное применение гепарина натрия в виде мази, геля, который 2-3 раза в сутки наносят тонким слоем на поврежденные участки (тромбофлебит поверхностных вен, постинъекционные флебиты, тромбоз геморроидальных вен) и, если это возможно, осторожно втирают. Гепарин натрия практически не абсорбируется из ЖКТ, но хорошо всасывается при подкожном введении.
Низкомолекулярные гепарины (НМГ) получают путем деполимеризации гепарина натрия, в них особое место занимают фракции с молекулярной массой менее 5400 Да и почти полностью отсутствуют крупномолекулярные компоненты (более 12 000 Да), преобладающие в обычном гепарине натрия. Основная качественная осо-
бенность НМГ состоит в том, что они преимущественно ингибируют фактор Ха (анти-Ха активность), а не тромбин (анти Па активность). По ряду свойств НМГ и гепарин натрия не отличаются друг от друга. Препараты не проникают трансплацентарно, оказывают стимулирующее влияние на фибринолиз - главным образом путем усиления выброса из эндотелия в кровь ТАП. К низкомолекулярным гепари-нам относят далтепарин натрия (фрагмин*), надропарин кальция (фраксипарин*) и эноксапарин (клексан*).
НМГ вводят подкожно - в область живота кнаружи от краев прямых мышц ниже уровня пупка. Из подкожной клетчатки эти препараты хорошо и быстро всасываются в кровь. Внутримышечные инъекции НМГ, как и гепарина натрия, противопоказаны, допустимо внутривенное введение (натриевые соли), но его применяют редко, в случаях необходимости получения немедленного антитромботиче-ского эффекта (в частности, при тромбоэмболии легочной артерии, остром ИМ).
Дозы НМГ измеряют в анти-Ха единицах. Единицы активности гепарина натрия и НМГ не соответствуют друг другу, и их нельзя перевести одни в другие. НМГ значительно дороже гепарина натрия.
НЛР. Самое частое осложнение гепаринотерапии - кровотечение. Частота кровотечений при лечении гепарином натрия колеблется в широких пределах, зависит от дозы препарата, способа его введения и некоторых других факторов. Риск возникновения кровотечений повышен у пожилых лиц, больных почечной или печеночной недостаточностью, а также при одновременном назначении с ацетилсалициловой кислотой и тромболитическими препаратами. Лечение гепарином натрия необходимо проводить под обязательным контролем коагулограммы (АЧТВ) в условиях стационара, в то время как назначение НМГ более безопасно с точки зрения развития кровотечений и не требует контроля АЧТВ. Препараты этой группы можно применять в амбулаторной практике.
При применении гепарина натрия возможно развитие тромбоцито-пении. Ранняя тромбоцитопения, возникающая в первые 3-4 сут применения препарата, как правило, умеренная (снижение тромбоцитов редко достигает 100409/л), протекает чаще всего бессимптомно и не дает осложнений. Значительно более серьезным осложнением считают развитие отсроченной иммунной тромбоцитопении (6-12 сут), характеризующейся более выраженным и стабильным снижением количества тромбоцитов, иногда осложняющимся геморрагиями и рикошетными
тромбозами. Это состояние требует немедленного отказа от дальнейшего введения гепарина натрия и перехода на другие методы антитромбо-тической профилактики. При введении НМГ частота тромбоцитопении ниже, чем при применении гепарина натрия.
Из других осложнений гепаринотерапии следует отметить остео-пороз, который становится диагностируемым при длительном применении препарата (более 2-4 нед), алопецию, аллергические реакции, повышение активности аминотрансфераз.
Противопоказания. Внутреннее кровотечение, геморрагический диатез, нарушение мозгового кровообращения по геморрагическому типу или хирургическое вмешательство на головном и спинном мозге, мочеполовых путях в последние 2 мес, неконтролируемая АГ, тяжелая почечная или печеночная недостаточность, варикозное расширение вен пищевода, подозрение на расслаивающую аневризму аорты или острый панкреатит, острый перикардит.
26.5. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ
АНТИКОАГУЛЯНТОВ НЕПРЯМОГО ДЕЙСТВИЯ
Антикоагулянтами непрямого действия (непрямые антикоагулянты) называют антитромботические препараты, нарушающие образование в печени активной формы витамина К, необходимого для синтеза предшественников протромбина и некоторых других факторов свертывания (факторы VII, IX, X). Непрямые антикоагулянты - конкурентные антагонисты витамина К1. Основными преимуществами этих препаратов считают возможность приема внутрь, что делает удобным их длительное применение как с лечебной целью, так и для профилактики тромбозов. К непрямым антикоагулянтам относят варфарин, аценокумарол (синкумар*) и фениндион (фенилин).
Фармакокинетика. Непрямые антикоагулянты на 80-90% абсорбируются при приеме внутрь, связываются с альбуминами плазмы на 99%, подвергаются биотрансформации в печени под влиянием CYP2C9 (варфарин и аценокумарол). Пути метаболизма фениндиона неизвестны. Неактивные метаболиты препаратов экскретируются почками. Препараты проникают через плаценту и могут вызвать геморрагические нарушения и аномалии развития у плода (изменения лицевого черепа).
Фармакодинамика. Непрямые антикоагулянты блокируют в гепа-тоцитах конечный этап образования витамин К-зависимых фак-
торов свертывания (факторов VII, X, IX, II) - карбоксилирование путем блокады фермента витамин К экпоксидредуктазы. В результате этого возникает гипокоагуляция, препятствующая появлению и прогрессированию тромбозов. Таким образом, непрямые антикоагулянты, так же, как дезагреганты и прямые антикоагулянты, останавливают рост тромбов и предотвращают образование новых. Антикоагулянтный эффект достигает максимума к 3-4-м суткам (аценокумарол) и к 5-6-м суткам (варфарин). При назначении вар-фарина и аценокумарола отмечают более стабильный антикоагулянт-ный эффект, чем при применении фениндиона.
При приеме непрямых антикоагулянтов в коагулограмме удлиняется протромбиновое время и повышается показатель МНО. Именно МНО считают основным показателем для индивидуального подбора дозы, контроля эффективности и безопасности непрямых антикоагулянтов. Считают, что непрямые антикоагулянты эффективно предотвращают образование тромбов при значениях МНО 2-3 (для больных с протезированными клапанами сердца - 2,5-4). Контроль МНО обязателен при применении непрямых антикоагулянтов, и, если он невозможен, препараты не назначают. В настоящее время появилась возможность контроля МНО в домашних условиях с помощью портативного прибора «Коагучек».
НЛР. При применении непрямых антикоагулянтов достаточно часто развиваются кровотечения (до 25% в год), включая опасные для жизни, такие как желудочно-кишечные и кровоизлияния в мозг. Риск кровотечений увеличивается при значениях МНО выше 4. Следовательно, основным методом профилактики кровотечений при применении непрямых антикоагулянтов можно считать только строгий контроль МНО. Индивидуальный выбор начальной дозы варфарина можно сделать на основе результатов фармакогенетиче-ского тестирования (см. гл. 9), что снижает риск кровотечений.
Непрямые антикоагулянты снижают активность не только факторов свертывания крови VII, IX, X II, но и двух важнейших физиологических антикоагулянтов - протеина С и S, что может стать причиной развития некрозов кожи в первые дни приема препаратов.
Противопоказания к применению. Непрямые антикоагулянты не назначают лицам старческого возраста (старше 80 лет), во время беременности и новорожденным, а также больным АГ высокой степени, тиреотоксикозом, с нарушениями мозгового кровообращения в ближайшем анамнезе, при наличии заболеваний, которые могут осложниться тяжелыми кровотечениями (язвенной болезни желудка
и двенадцатиперстной кишки, эрозивного гастрита, язвенного колита, геморрагических диатезов), при серьезных заболеваниях печени, больших травмах и хирургических вмешательствах.
Взаимодействие с другими ЛС. На эффективность применения непрямых антикоагулянтов влияют различные факторы, в том числе и множество ЛС. Их действие усиливают алкоголь, клюквенный сок, ацетилсалициловая кислота, НПВС, амиодарон, пенициллины, ампициллин, тетрациклины, хлорамфеникол, фторхинолоны, дигоксин, статины, тироксин, трициклические антидепрессанты, фитопрепараты (препараты чеснока, гинкго билоба, клюквы), коэнзим Q и другие препараты. Ослабляют действие непрямых антикоагулянтов продукты, богатые витамином К (зеленые овощи: салат, шпинат), барбитураты, галоперидол, глюкокортикоиды, рифампицин, поливитамины.
Антикоагулянты непрямого действия могут усиливать гипоглике-мическое действие препаратов сульфонилмочевины, ульцерогенный эффект глюкокортикоидов.
26.6. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ ТРОМБОЛИТИЧЕСКИХ СРЕДСТВ
В отличие от антитромбоцитарных препаратов, прямых и непрямых антикоагулянтов, действие которых направлено на предотвращение тромбообразования, механизм действия тромболитических средств заключается в растворении фибринового тромба и восстановлении кровотока в соответствующем органе или его части - при остром ИМ, ТЭЛА, инфаркте мозга. Тромболитические препараты применяют только в условиях реанимационных отделений стационаров.
Для тромболизиса необходимо повысить фибринолитическую активность крови больного, что можно достигнуть двумя путями:
- введением активированного плазмина, тем самым увеличивая его концентрацию в крови;
- введением активаторов плазминогена, которые усиливают образование плазмина из эндогенного плазминогена.
Наиболее употребляемые в настоящее время тромболитические препараты по механизму действия представляют собой активаторы эндогенного плазминогена (табл. 26-4).
• Стрептокиназа - гетерогенный активатор плазминогена, получаемый из некоторых штаммов стрептококков или рекомбинант-но.
• Урокиназа - фермент, который непосредственно превращает плаз-миноген в плазмин; проурокиназа (одноцепочечная урокиназа).
• Тканевый (эндотелиальный) активатор плазминогена - ТАП (алтеплаза).
• Тенектеплаза - создана с помощью генной инженерии путем замены аминокислотных остатков в трех участках исходной молекулы ТАП.
Таблица 26-4. Сравнительная характеристика основных тромболитических
препаратов
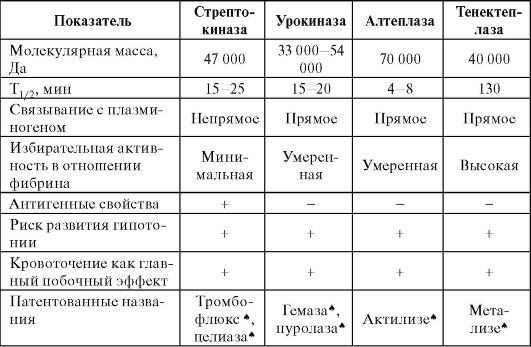
Стрептокиназа активирует плазминоген как в тромбе, так и в крови, и этот препарат наиболее часто вызывает кровотечения. Стрептокиназа - очень аллергогенный препарат: при его введении часто развиваются аллергические реакции вплоть до анафилактического шока. Кроме того, у пациентов со стрептококковыми инфекциями в анамнезе или при повторном введении стрептокиназы эффективность лечения может снижаться путем блокирования препарата антителами. Урокиназа, получаемая из культуры клеток почечной ткани человека, лишена аллергогенных свойств, но частота кровотечений при ее применении сопоставима со стрептокиназой. Алтеплаза (генно-инженерный аналог ТАП) действует преимущественно в тромбе и благодаря этому реже вызывает аллергические реакции и крово-
течения. Стрептокиназу, урокиназу и алтеплазу вводят внутривенно с последующим внутривенным капельным введением. Тенектеплаза, кроме других преимуществ алтеплазы, обладает более длительным периодом полувыведения, а значит, действует дольше и ее можно вводить внутривенно болюсно однократно, без необходимости поддерживающей внутривенной капельной инфузии.
Противопоказания к проведению тромболизиса - продолжающееся кровотечение, недавнее (последние 10 сут) кровотечение, хирургическое вмешательство или травма, состояния, при которых высока вероятность кровоизлияния в мозг (диагностированная опухоль мозга, первые 3 мес после геморрагического инсульта, черепно-мозговой травмы или нейрохирургического вмешательства), геморрагический диатез, расслаивающая аневризма аорты.
26.7. ГЕМОРРАГИЧЕСКИЙ СИНДРОМ
Геморрагический синдром встречается при различных состояниях, сопровождающихся нарушениями гемостаза, и проявляется повышенной кровоточивостью. Можно выделить целый ряд заболеваний, сопровождающихся геморрагическим синдромом.
• Наследственная недостаточность отдельных факторов свертывания. Например, гемофилия A - редкое (1:50 000 новорожденных), сцепленное с полом1, заболевание, связанное с отсутствием в крови больных фактора свертывания VIII. Клинически проявляется подкожными гематомами и длительными кровотечениями после порезов. Гемофилия В связана с недостаточностью фактора IX, а гемофилия C - c отсутствием фактора XI.
• Нарушение функции эндотелия и синтеза фактора VIII (болезнь Виллебранда).
• Аутоиммунная тромбоцитопения - хроническое рецидивирующее заболевание, связанное с повышенным разрушением тромбоцитов. Для заболевания характерно снижение количества тромбоцитов менее 50-109-л-1. Проявляется подкожными кровоизлияниями, кровотечениями из слизистых оболочек.
• Геморрагические васкулиты - группа заболеваний, для которых характерны тромбозы и геморрагии мелких сосудов, вызванные повреждением эндотелия иммунными комплексами.
1 Болеют только лица мужского пола.
• Передозировка антикоагулянтов, дезагрегантов или активаторов фибринолиза.
• Наследственная патология соединительной ткани (нарушения строения сосудистой стенки).
• Тяжелые заболевания печени (цирроз печени), сопровождающиеся недостаточностью факторов свертывания, синтезируемых в печени.
Синдром диссеминированного внутрисосудистого свертывания крови
ДВС-синдром - это состояние, при котором процесс тромбооб-разования в силу ряда причин не ограничивается поврежденными участками сосудов, а разворачивается диффузно во всем организме. При этом быстро развивается дефицит тромбоцитов и плазменных факторов свертывания, что приводит к повышенной кровоточивости. Без лечения ДВС-синдром протекает с развитием недостаточности различных органов, в которых произошли тромбозы, с другой стороны, процесс может сопровождаться опасными для жизни кровотечениями. Наиболее частыми причинами ДВС-синдрома становятся тяжелые инфекции, сепсис, травмы и шок.
Основные симптомы геморрагических состояний. Симптомы геморрагических состояний очень разнообразны и зависят от характера и тяжести заболевания:
- образование гематом - болезненных, напряженных кровоизлияний в мягкие ткани или в суставы (типично для гемофилии А и В);
- образование петехий (точечные кровоизлияния) - характерно для тромбоцитопений и наследственного дефицита факторов
Х, II и VII;
- одновременное появление у больных гематом и петехий наблюдают при болезни Виллебранда, ДВС-синдроме, передозировке антикоагулянтов и тромболитиков;
- геморрагии в виде сыпи или эритемы (на коже) с гематурией1 и кишечными кровотечениями, наблюдают при инфекционных и иммунных васкулитах2;
1 Гематурия - наличие крови в моче.
2 Васкулит - воспалительные заболевания сосудов различного происхождения. Наиболее часто васкулиты встречаются при тяжелых инфекциях (например, менинго-кокковые инфекции) и системных заболеваниях соединительной ткани.
- кровотечения различных локализаций отмечают при заболеваниях, протекающих с разрушением (деструкцией) органов и тканей, - в первую очередь это злокачественные новообразования (наличие крови в каловых массах обычно становится первым симптомом опухолей ЖКТ) и инфекции (например, легочные кровотечения при туберкулезе). Диагностика геморрагического синдрома заключается в оценке состояния гемостаза и диагностике первичного заболевания, приводящего к кровоточивости.
Клинико-фармакологический подход к выбору препаратов для лечения кровотечений представлен в табл. 26-5.
Таблица 26-5. Клинико-фармакологические подходы к лечению кровотечений
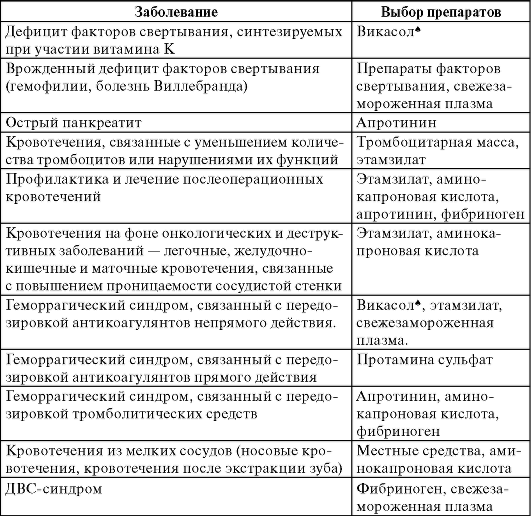
Для остановки кровотечения при гемофилии А в пред- и операционном периоде применяют антигемофильную плазму, криопреци-питат, концентрат фактора VIII.
При гемофилии В внутривенно струйно вводят свежезамороженную плазму в дозе 15-20 мг/кг 1 раз в сутки, стремясь к увеличению концентрации фактора IX в крови на 10-15%. Применяют концентрат фактора IX, в том числе и для профилактики кровотечений.
При болезни Виллебранда для лечения и профилактики кровотечений, подготовки и проведения операций назначают криопреципи-тат или свежезамороженную плазму.
Противозачаточные средства используют для профилактики и ограничения менструальных кровотечений.
При кровотечениях, связанных с дефицитом витамина К, применяют препараты витамина К. При передозировке непрямых антикоагулянтов больным назначают инъекции викасола*, возможно назначение трансфузии свежезамороженной плазмы.
При геморрагиях, связанных с нарушением проницаемости сосудистой стенки, вводят этамзилат. Этот препарат назначают при гинекологических операциях для ограничения объема кровопотери, в урологической практике до и во время простатэктомии, в стоматологической хирургии (экстракция зубов), для лечения кровоизлияний на глазном дне. Кроме того, препарат способствует остановке желудочно-кишечных, легочных кровотечений, эффективен при передозировке кумариновых препаратов.
Передозировка гепарина натрия и связанные с этим кровотечения купируют внутривенным введением протамина сульфата.
При передозировке тромболитиков для остановки кровотечения применяют неспецифический ингибитор сериновой протеазы - апротинин (трасилол*, контрикал*), аминокапроновую кислоту, фибриноген, препараты крови.

