Адиабатический процесс (адиабатный процесс) - термодинамический процесс, происходящий в системе без теплообмена с окружающей средой (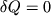 ), т. е. в адиабатически изолированной системе, состояние которой можно изменить только путем изменения внешних параметров. Понятие адиабатической изоляции является идеализацией теплоизолирующих оболочек или сосудов Дьюара (адиабатные оболочки). Изменение температуры внешних тел не оказывает влияния на адиабатически изолированной системы, а их энергия U может изменяться только за счет работы, совершаемой системой (или над ней). Согласно первому началу термодинамики, при обратимом адиабатическом процессе для однородной системы
), т. е. в адиабатически изолированной системе, состояние которой можно изменить только путем изменения внешних параметров. Понятие адиабатической изоляции является идеализацией теплоизолирующих оболочек или сосудов Дьюара (адиабатные оболочки). Изменение температуры внешних тел не оказывает влияния на адиабатически изолированной системы, а их энергия U может изменяться только за счет работы, совершаемой системой (или над ней). Согласно первому началу термодинамики, при обратимом адиабатическом процессе для однородной системы 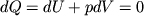 , где V - объем системы, p - давление, а в общем случае
, где V - объем системы, p - давление, а в общем случае 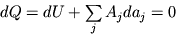 , где aj, - внешние параметры, Аj - термодинамические силы. Согласно второму началу термодинамики, при обратимом адиабатическом процессе энтропия постоянна,
, где aj, - внешние параметры, Аj - термодинамические силы. Согласно второму началу термодинамики, при обратимом адиабатическом процессе энтропия постоянна, 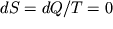 , а при необратимом - возрастает. Очень быстрые процессы, при которых не успевает произойти теплообмен с окружающей средой, например, при распространении звука, можно рассматривать как адиабатический процесс. Энтропия каждого малого элемента жидкости при его движении со скоростью v остается постоянной, поэтому полная производная энтропии s, отнесенной к единице массы, равна нулю,
, а при необратимом - возрастает. Очень быстрые процессы, при которых не успевает произойти теплообмен с окружающей средой, например, при распространении звука, можно рассматривать как адиабатический процесс. Энтропия каждого малого элемента жидкости при его движении со скоростью v остается постоянной, поэтому полная производная энтропии s, отнесенной к единице массы, равна нулю, 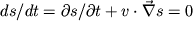 (условие адиабатичности). Простым примером адиабатического процесса является сжатие (или расширение) газа в теплоизолированном цилиндре с теплоизолированным поршнем: при сжатии температуpa возрастает, при расширении - убывает. Другим примером адиабатического процесса может служить адиабатическое размагничивание, которое используют в методе магнитного охлаждения. Обратимый адиабатический процесс, называется также изоэнтропийным, изображается на диаграмме состояния
(условие адиабатичности). Простым примером адиабатического процесса является сжатие (или расширение) газа в теплоизолированном цилиндре с теплоизолированным поршнем: при сжатии температуpa возрастает, при расширении - убывает. Другим примером адиабатического процесса может служить адиабатическое размагничивание, которое используют в методе магнитного охлаждения. Обратимый адиабатический процесс, называется также изоэнтропийным, изображается на диаграмме состояния
Адиабатический процесс - это такое изменение состояний газа, при котором он не отдает и не поглощает извне теплоты. Следовательно, адиабатический процесс характеризуется отсутствием теплообмена газа с окружающей средой. Адиабатическими можно считать быстро протекающие процессы. Так как передачи теплоты при адиабатическом процессе не происходит, то  и уравнение I начала термодинамики принимает вид
и уравнение I начала термодинамики принимает вид
 |
(9.20) |
или
т.е. внешняя работа газа может производиться вследствие изменения его внутренней энергии. Адиабатное расширение газа (dV>0) сопровождается положительной внешней работой, но при этом внутренняя энергия уменьшается и газ охлаждается (dT<0).
Сжатие газа (dV0, т.е. адиабатное сжатие газа сопровождается его нагреванием.
Найдем связь между параметрами состояния идеального газа (например, Р и V) в адиабатическом процессе. Для этого перепишем (9.20) в форме

а величину  найдем из уравнения Менделеева - Клапейрона
найдем из уравнения Менделеева - Клапейрона

Таким образом,
или, учитывая, что для идеального газа 

Разделим обе части этого уравнения на 

где  безразмерная величина, называемая постоянной адиабаты. Пренебрегая зависимостью
безразмерная величина, называемая постоянной адиабаты. Пренебрегая зависимостью  от температуры, можно считать, что для данного газа
от температуры, можно считать, что для данного газа  . Интегрируя последнее уравнение
. Интегрируя последнее уравнение

получим
т.е.
 |
(9.21) |
Это выражение называют уравнением Пуассона. Соотношение между давлением и температурой, а также между объемом и температурой идеального газа в адиабатическом процессе имеют вид

Эти соотношения легко получить из (9.21), пользуясь уравнением Менделеева - Клапейрона. Линию, изображающую адиабатический процесс в диаграмме состояния, называют адиабатой. На рис. 9.7 сплошной линией показан вид адиабаты в (P-V) диаграмме. Для сравнения в том же рисунке пунктирной линией изображена изотерма, соответствующая температуре газа в начальном состоянии 1. Так как для любого идеального газа показатель адиабаты  , то в (P-V) диаграмме адиабата всегда идет круче, чем изотерма. Объясняется это тем, что при адиабатическом сжатии увеличение давления обусловлено не только уменьшением объема газа, как при изотермическом сжатии, то также еще и увеличения температуры. При адиабатическом расширении температура газа уменьшается, поэтому давление газа падает быстрее, чем при изотермическом расширении.
, то в (P-V) диаграмме адиабата всегда идет круче, чем изотерма. Объясняется это тем, что при адиабатическом сжатии увеличение давления обусловлено не только уменьшением объема газа, как при изотермическом сжатии, то также еще и увеличения температуры. При адиабатическом расширении температура газа уменьшается, поэтому давление газа падает быстрее, чем при изотермическом расширении.

Работу, совершаемую газом в адиабатическом процессе, найдем интегрируя выражение

Полная работа
Из уравнения Майера (9.18) и выражения  для показателя адиабаты γ следует, что
для показателя адиабаты γ следует, что

Поэтому
 |
(9.22) |
В соответствии с соотношением 

Следовательно, выражение (9.22) для работы можно представить в виде

или

