{Молярная теплоемкость газа для изопроцессов}
Теплоёмкость идеального газа — отношение количества теплоты, сообщённого газу, к изменению температуры δТ, которое при этом произошло.
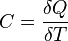
Молярная теплоёмкость
Молярная теплоёмкость — теплоёмкость 1 моля идеального газа.


Теплоёмкость идеального газа в изопроцессах
Адиабатический
В адиабатическом процессе теплообмена с окружающей средой не происходит, то есть  . Однако, объём, давление и температура меняются, то есть
. Однако, объём, давление и температура меняются, то есть  .
.
Следовательно, теплоёмкость идеального газа в адиабатическом процессе равна нулю:  .
.
Изотермический
В изотермическом процессе постоянна температура, то есть 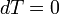 . При изменении объёма газу передаётся (или отбирается) некоторое количество тепла. Следовательно, теплоёмкость идеального газа равна минус бесконечности:
. При изменении объёма газу передаётся (или отбирается) некоторое количество тепла. Следовательно, теплоёмкость идеального газа равна минус бесконечности: 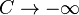
Изохорный
В изохорном процессе постоянен объём, то есть  . Элементарная работа газа равна произведению изменения объёма на давление, при котором происходит изменение (
. Элементарная работа газа равна произведению изменения объёма на давление, при котором происходит изменение (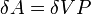 ). Первое Начало Термодинамики для изохорного процесса имеет вид:
). Первое Начало Термодинамики для изохорного процесса имеет вид:

А для идеального газа

Таким образом,

где 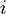 — число степеней свободы частиц газа.
— число степеней свободы частиц газа.
Другая формула:  , где γ — показатель адиабаты, R — универсальная газовая постоянная.
, где γ — показатель адиабаты, R — универсальная газовая постоянная.
Изобарный
Молярная теплоёмкость при постоянном давлении обозначается как  . В идеальном газе она связана с теплоёмкостью при постоянном объёме соотношением Майера
. В идеальном газе она связана с теплоёмкостью при постоянном объёме соотношением Майера 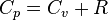 .
.
Молекулярно-кинетическая теория позволяет вычислить приблизительные значения молярной теплоёмкости для различных газов через значение универсальной газовой постоянной:
- для одноатомных газов
 , то есть около 20.8 Дж/(моль·К);
, то есть около 20.8 Дж/(моль·К); - для двухатомных газов
 , то есть около 29.1 Дж/(моль·К);
, то есть около 29.1 Дж/(моль·К); - для многоатомных газов
 , то есть около 33.3 Дж/(моль·К).
, то есть около 33.3 Дж/(моль·К).
Теплоёмкости можно также определить исходя из уравнения Майера, если известен показатель адиабаты, который можно измерить экспериментально (например, с помощью измерения скорости звука в газе или используя метод Клемана — Дезорма).

