1. В отличие от оптических линейчатых спектров с их сложностью и разнообразием, рентгеновские характеристические спектры различных элементов отличаются простотой и однообразием. С ростом атомного номера Z элемента они монотонно смещаются в коротковолновую сторону.
2. Характеристические спектры разных элементов имеют сходный характер (однотипны) и не меняются, если интересующий нас элемент находится в соединении с другими. Это можно объяснить лишь тем, что характеристические спектры возникают при переходах электронов во внутренних частях атома, частях, имеющих сходное строение.
3. Характеристические спектры состоят из нескольких серий: К, L, М, ... Каждая серия — из небольшого числа линий: Ка, Кβ, Кγ, ... La, Lβ, Ly, ... и т. д. в порядке убывания длины волны λ.
Схема возникновения характеристических спектров. Возбуждение атома возникает при удалении одного из внутренних электронов. Если вырывается один из двух электронов K-уровня (n = 1), то освободившееся место может быть занято электроном из какого-либо более высокого уровня: L, M, N, и т. д. В результате возникает K-серия. Подобным же образом возникают и другие серии: L, М, ...
С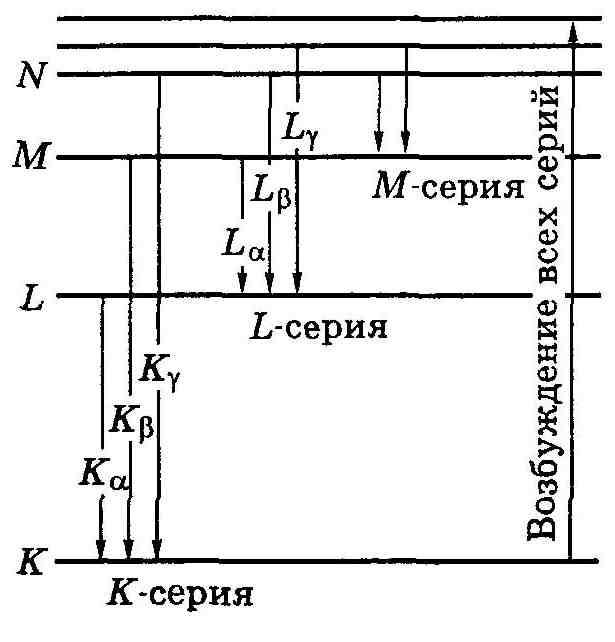 ерияК, как видно из рис.13.6, непременно сопровождается появлением и остальных серий, поскольку при испускании ее линий освобождаются электроны на уровнях L, М и др., которые в свою очередь будут заполняться электронами с более высоких уровней.
ерияК, как видно из рис.13.6, непременно сопровождается появлением и остальных серий, поскольку при испускании ее линий освобождаются электроны на уровнях L, М и др., которые в свою очередь будут заполняться электронами с более высоких уровней.
Молекулярные спектры.
Молекулярные спектры - оптические спектры испускания и поглощения, а также комбинационного рассеяния света , принадлежащие свободным или слабо связанным между собой Молекулам. М. с. имеют сложную структуру. Типичные М. с. — полосатые, они наблюдаются в испускании и поглощении и в комбинационном рассеянии в виде совокупности более или менее узких полос в ультрафиолетовой, видимой и близкой инфракрасной областях, распадающихся при достаточной разрешающей силе применяемых спектральных приборов на совокупность тесно расположенных линий. Конкретная структура М. с. различна для различных молекул и, вообще говоря, усложняется с увеличением числа атомов в молекуле. Для весьма сложных молекул видимые и ультрафиолетовые спектры состоят из немногих широких сплошных полос; спектры таких молекул сходны между собой.
Из решения уравнения Шредингера для молекул водорода при указанных выше предположениях получается зависимость собственных значений энергии от расстояния R между ядрами, т. е. Е = E(R).
Энергия молекулы
|
Е ≈ Еэл + Екол + Евращ, |
(13.45) |
где Еэл — энергия движения электронов относительно ядер; Екол — энергия колебаний ядер (в результате которых периодически изменяется относительное положение ядер); Евращ — энергия вращения ядер (в результате которых периодически изменяется ориентация молекулы в пространстве).
Доказано, что Еэл >> Екол >> Евращ, при этом Еэл ≈ 1 – 10 эВ. Каждая из входящих в выражение (13.45) энергий квантуется и им соответствует набор дискретных уровней энергии.Расстояние между вращательными уровнями энергии Δ Евращ гораздо меньше расстояния между колебательными уровнями Δ Екол, которое, в свою очередь, меньше расстояния между электронными уровнями Δ Еэл.
Строение молекул и свойства их энергетических уровней проявляются в молекулярных спектрах - спектрах излучения , возникающих при квантовых переходах между уровнями энергии молекул. Спектр излучения молекулы определяется структурой ее энергетических уровней и соответствующими правилами отбора . При разных типах переходов между уровнями возникают различные типы молекулярных спектров. Частоты спектральных линий, испускаемых молекулами, могут соответствовать переходам с одного электронною уровня на другой или с одного колебательного (вращательного) уровня на другой
Кроме того, возможны и переходы с одними значениями Екол и Евращ на уровни, имеющие другие значения всех трех компонентов, в результате чего возникают электронно-колебательные и колебательно-вращательные спектры. Поэтому спектр молекул довольно сложный.
Типичные молекулярные спектры - полосатые, представляют собой совокупность более или менее узких полос в ультрафиолетовой, видимой и инфракрасной областях. Применяя спектральные приборы высокой разрешающей способности, можно видеть, что полосы представляют собой настолько тесно расположенные линии, что они с трудом разрешаются.
Структура молекулярных спектров различна для разных молекул и с увеличением числа атомов в молекуле усложняется . Колебательными и вращательными спектрами обладают только многоатомные молекулы, а двухатомные их не имеют.
Молекулярные спектры применяются для исследования строения и свойств молекул, используются в молекулярном спектральном анализе, лазерной спектроскопии, квантовой электронике и т.д.
ВИДЫ СВЯЗЕЙ В МОЛЕКУЛАХ Химическая связь — явление взаимодействия атомов, обусловленное перекрыванием электронных облаков связывающихся частиц, которое сопровождается уменьшениемполной энергии системы. Ионная связь — прочная химическая связь, образующаяся между атомами с большой разностью электроотрицательностей, при которой общаяэлектронная пара полностью переходит к атому с большей электроотрицательностью.Это притяжение ионов как разноименно заряженных тел. Электроотрицательность (χ) — фундаментальное химическое свойство атома, количественная характеристика способности атома в молекуле смещать к себе общие электронные пары. Ковалентная связь (атомная связь, гомеополярная связь) — химическая связь, образованная перекрытием (обобществлением) пары валентных электронных облаков. Обеспечивающие связь электронные облака (электроны) называются общей электронной парой.Водородная связь — связь между электроотрицательным атомом и атомом водорода H, связанным ковалентно с другим электроотрицательным атомом. Металлическая связь — химическая связь, обусловленная наличием относительно свободных электронов. Характерна как для чистых металлов, так и их сплавов иинтерметаллических соединений.

