Прежде всего, в экспериментах было замечено, что линии в спектрах расположены не беспорядочно, а сериями. Расстояние между линиями в серии закономерно уменьшается по мере перехода от длинных волн к коротким.
Самым простым и наиболее изученным является спектр атома водорода. Анализ эмпирического материала показал, что отдельные линии в спектре могут быть объединены в группы линий, которые называются сериями. В 1885 г. И.Бальмер установил, что частоты 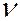 линий в видимой части спектра водорода можно представить в виде простой формулы:
линий в видимой части спектра водорода можно представить в виде простой формулы:
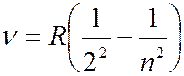 (
( 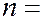 3, 4, 5, … ),
3, 4, 5, … ),  (7.42.1)
(7.42.1)
где 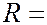 3,29∙1015 с-1 – постоянная Ридберга. Спектральные линии, отличающиеся различными значениями
3,29∙1015 с-1 – постоянная Ридберга. Спектральные линии, отличающиеся различными значениями 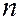 , образуют серию Бальмера.
, образуют серию Бальмера.
Серия Лаймона  , n = 2, 3, 4,…
, n = 2, 3, 4,…
Серия Пашена  ,n = 4, 5, 6,…
,n = 4, 5, 6,…
Серия Брэкета  , n = 5, 6, 7,…
, n = 5, 6, 7,…
Серия Пфунда  , n = 6, 7, 8,…
, n = 6, 7, 8,…

