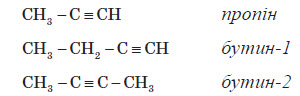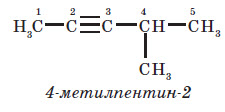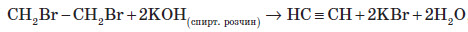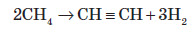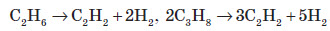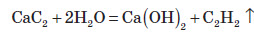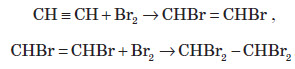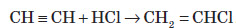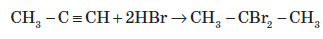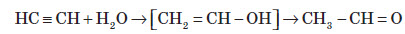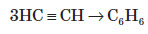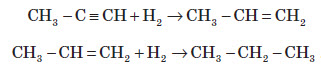Гомологічний ряд алкінів
Алкінами називають ненасичені вуглеводні, молекули яких мають один потрійний зв’язок. Перший представник цього класу — ацетилен HC = CH, у зв’язку із чим алкіни також називають ацетиленовими вуглеводнями. Найближчі гомологи ацетилену:
Загальна формула гомологічного ряду алкінів CnH2n-2 . Вона збігається із загальною формулою алкадієнів, тому алкіни й алкадієни є міжкласовими ізомерами.
Ізомерія й номенклатура
Структурна ізомерія алкінів обумовлена ізомерією карбонового кістяка, так само як і в алканів та алкенів (наприклад, 3-метилбутин-1 і пентин-1), та ізомерією положення потрійного зв’язку (бутин-1 і бутин-2). Просторова ізомерія для алкінів не характерна. В алкінах з нерозгалуженим карбоновим ланцюгом нумерацію починають із того кінця, ближче до якого перебуває потрійний зв’язок. У назві відповідного алкану закінчення -ан змінюється на -ін (-ин).
У розгалужених алкінах вибирають головний ланцюг так, щоб він містив потрійний зв’язок, навіть якщо він при цьому й не буде найдовшим. Перед назвою головного ланцюга вказують номер атома Карбону, при якому перебуває замісник, і назву цього замісника. Номер після назви головного ланцюга вказує положення по трійного зв’язку, наприклад:
Будова алкінів
Атоми Карбону при потрійному зв’язку перебувають у стані sp-гібридизації. Два σ-зв’язки, утворені гібридними орбіталями, розташовуються вздовж однієї лінії під кутом 180° один щодо одного; два п-зв’язки утворені при перекриванні двох пар негібридних p-орбіталей сусідніх атомів Карбону. Додаткове зв’язування двох атомів Карбону призводить до того, що відстань між ядрами зменшується, оскільки потрійний зв’язок є поєднанням одного σ-зв’язку і двох п-зв’язків. Довжина потрійного зв’язку C = C становить 0,121 нм, що менше за довжину як одинарного, так і подвійного зв’язку. Енергія потрійного зв’язку становить 828 кДж / моль.
Добування алкінів
1. Загальний спосіб добування алкінів — відщеплення двох молекул галогеноводню від дигалогеналканів, які містять два атоми галогену або в сусідніх, або в одного атома Карбону, під дією спиртового розчину лугу:
2. У промисловості ацетилен добувають шляхом високотемпературного крекінгу метану:
або його найближчих гомологів — етану й пропану, причому в цьому разі ацетилен утворюється при більш низьких температурах 1200 °С:
Сировиною в цих способах є природний газ або нафта.
3. У лабораторних умовах ацетилен добувають гідролізом кальцій карбіду:
Хімічні властивості алкінів
Реакції приєднання для алкінів протікають повільніше, ніж для алкенів.
1. Галогенування. Галогени приєднуються до алкінів у дві стадії:
Алкіни, так само як і алкени, знебарвлюють бромну воду.
2. Гідрогалогенування. Галогеноводні приєднуються до потрійного зв’язку важче, ніж до подвійного:
У разі надлишку галогеноводню відбувається повне гідрогалогенування, причому для несиметричних алкінів на кожній стадії приєднання йде за правилом Марковникова, наприклад:
3. Гідратація. Приєднання води до алкінів каталізується солями ртуті (II):
Реакцію гідратації алкінів відкрив М. Г. Кучеров (1881 р.), саме тому її й називають реакцією Кучерова.
4. Полімеризація. При пропусканні ацетилену над активованим вугіллям при температурі +600 °С
відбувається тримеризація ацетилену з утворенням бензену:
5. Реакції відновлення. У присутності металевих каталізаторів алкіни відновлюються шляхом послідовного приєднання молекул водню, перетворюючись спочатку в алкени, а потім в алкани: