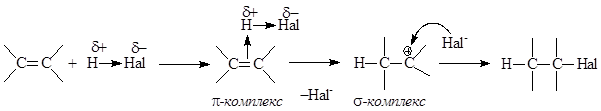
При взаимодействии алкенов с галогеноводородами лимитирующей стадией является присоединение протона через образование p-комплекса; реакция оканчивается последующей атакой образовавшегося карбкатиона галогенид-ионом. По мере увеличения кислотности легкость присоединения галогеноводородов возрастает в ряду: HF<HCl<HBr<HI.
В случае алкенов несимметричного строения, например, пропена, бутена-1, 2-метилпропена, присоединение галогеноводородов может приводить к образованию двух продуктов. На практике наблюдается региоселективное протекание реакции согласно правилу Марковникова: при взаимодействии несимметричных алкенов (алкинов, диенов) с соединениями типа Н-Х, атом Н присоединяется к более гидрогенизированному атому углерода при двойной (тройной) связи, а Х – к менее гидрогенизированному атому углерода. Есть и другие формулировки этого правила: присоединение протона к несимметричным алкенам идет с образованием более стабильного карбкатиона.
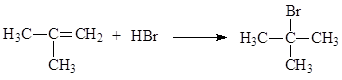
Механизм реакции:
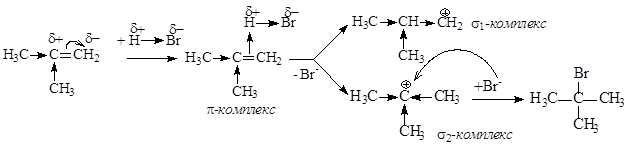
Региоселективное протекание реакции объясняют влиянием двух факторов – статического и динамического. Статический фактор рассматривает распределение электронной плотности в молекуле субстрата и, исходя из этого, определяет направление электрофильного присоединения. В нашем случае протон должен присоединяться к тому атому углерода при двойной связи, на котором имеется частичный отрицательный заряд, с образованием s2–комплекса. Динамический фактор рассматривает устойчивость образующихся интермедиатов (промежуточных продуктов) – карбкатионов (s –комплексов). Согласно динамическому фактору должно идти образование более стабильного интермедиата, для образования которого требуются меньшие затраты энергии, т.е. в реакции должен образовываться более стабильный третичный карбкатион (s2–комплекс). В приведенном примере оба фактора действуют согласованно, однако в случае несогласованного действия этих факторов главную роль играет динамический фактор. Оба фактора действуют согласованно и в случае гидрохлорирования 3,3,3-трифторпропена:
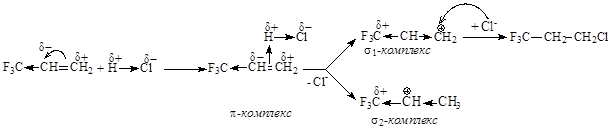
Реакционная способность 3,3,3-трифторпропена понижена из-за наличия в молекуле электроноакцепторной трифторметильной группы, что приводит к возникновению на вторичном атоме углерода частичного отрицательного заряда, а на первичном – частичного положительного. Исходя из распределения электронной плотности в субстрате можно предполагать, что протон должен присоединяться к менее гидрогенизированному атому углерода при двойной связи, с образованием первичного карбкатиона (s1–комплекса). Альтернативное присоединение протона должно приводить к возникновению вторичного карбкатиона (s2–комплекса). В данном случае менее стабильным оказывается именно вторичный карбкатион из-за близости атомов углерода с положительными зарядами. Большая стабильность первичного карбкатиона в этом случае объясняется удаленным расположением атомов, несущих положительные заряды. Таким образом, оба фактора и в этом случае действуют согласованно, реакция идет региоселективно, приводя к образованию 1,1,1-трифтор-3-хлорпропана.

