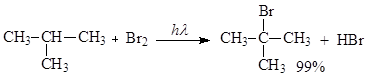В реакциях радикального замещения выделяют несколько последовательных стадий: инициирования, рост цепи, обрыв цепи. Рассмотрим подробнее на примере реакции хлорирования этана:
СН3-СН3 +Сl2 ® CH3-CH2-Cl + HCl
Инициирование:
Сl : Cl ® Cl× + Cl×
На этой стадии под действием кванта тепловой или световой энергии происходит гомолитический разрыв связи в молекуле хлора.
Рост цепи:
Cl× + СН3-СН3® CH3-CH2× +HCl
CH3-CH2× + Сl : Cl ® CH3-CH2-Cl + ×Cl
Cl× + СН3-СН3® CH3-CH2× +HCl
CH3-CH2× + Сl : Cl ® CH3-CH2-Cl + ×Cl
Образовавшиеся атомы хлора (свободные радикалы), стремясь завершить свой внешний электронный слой, отрывают атом водорода от молекулы этана. Отрыв атома водорода от молекулы алкана идет гомолитически, при этом образуются молекула хлороводорода и этильный (алкильный радикал). Образующийся углеводородный радикал отрывает атом хлора от молекулы Cl2, что приводит к образованию хлорэтана и радикала хлора, который далее вступает в реакцию с этаном. Таким образом одна реакция порождает другую и представляет собой цепь последовательных превращений. На этом этапе идет образование основных продуктов реакции.
Обрыв цепи:
Cl× + ×Cl ® Сl : Cl
CH3-CH2× + ×Cl ® CH3-CH2-Cl
CH3-CH2×+ CH3-CH2× ® СН3-СН3 + СН2=СН2
CH3-CH2× + ×CН2-СН3 ® CH3-CH2- CН2-СН3
По мере превращения исходных веществ в продукты реакции увеличивается вероятность взаимодействия радикалов между собой, что приводит к образованию молекул исходных веществ либо побочных продуктов. Эти процессы приводят к исчезновению из реакционной сферы свободных радикалов, в результате рост цепи прекращается.
Реакционная способность галогенов уменьшается от фтора к брому. Йод с алканами не реагирует вследствие эндотермичности такого процесса. Если в молекуле алкана содержатся первичные, вторичные и третичные атомы углерода, то под действием почти всех радикалов отрываются в первую очередь атомы водорода от третичного атома углерода, затем от вторичного и в последнюю очередь от первичного. Это согласуется энергиями связей: Е(Н-Стр) = 381 кДж/моль, Е(Н-Свт) = 393 кДж/моль, Е(Н-Сп) = 406 кДж/моль. В пользу такого протекания реакции свидетельствует устойчивость радикалов, которая уменьшается от третичного к первичному. Проведение реакций с хлором и фтором приводит к образованию смеси продуктов монозамещения, так как эти атомы обладают высокой реакционной способностью и легко разрывают любые связи Н-С. Однако в смеси продуктов содержание продукта замещения у третичного атома углерода большее, чем следовало ожидать из статистического подхода (ожидаемое количество 2-метил-2-хлорпропана – 10%, 2-метил-1-хлорпропана – 90%).
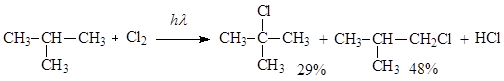
В случае реакции алканов с менее реакционноспособным радикалом брома, а потому и более избирательным, замещение протекает главным образом у третичного атома углерода, т.е. региоселективно. Региоселективность – это протекание реакции по одному из нескольких возможных реакционных центров.