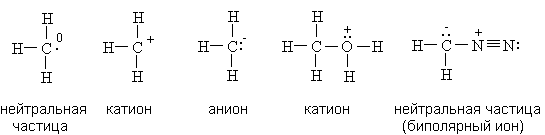
Г.Льюисом и В.Косселем (1916 г.) была предложена электронная теория химической связи. Согласно этой теории ковалентная связь образуется за счет пары электронов, общей для двух связываемых атомов. Частица устойчива, если валентная оболочка элементов первого периода (Н) содержит два (правило дублета), а элементов второго периода (C, N, O, F) - восемь электронов (правило октета).
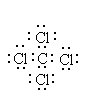
Электронное строение органических соединений изображают с помощью электронных формул Льюиса. В них с помощью точек указывают положение всех валентных электронов: электронов химических связей и неподеленных пар электронов. При этом считают, что неподеленные пары электронов составляют часть внешней оболочки только одного атома, а электроны, участвующие в образовании ковалентной связи, являются частью внешней оболочки обоих атомов. Например, в приведенной ниже формуле Льюиса для тетрахлорметана все атомы имеют октет электронов.
Для каждого атома в структуре Льюиса определяют формальный заряд. При этом полагают, что атому принадлежат все неподеленные электроны и половина электронов ковалентных связей. Избыток электронов, принадлежащих атому в молекуле по сравнению со свободным атомом, обусловливает отрицательный заряд, а недостаток - положительный заряд. Сумма формальных зарядов всех атомов дает заряд частицы в целом.