Алкилирование. Арены вступают в реакции алкилирования при участии комплексов алкилгалогенида с галогенидами металлов - AlCl3, FeCl3, ZnCl2 и др.
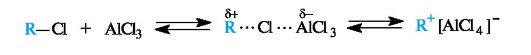
Реакция алкилирования представляет собой общий способ получения гомологов бензола - алкилбензолов.
Алкилирование часто не останавливается на стадии монозамещения и протекает дальше, поскольку введение первой алкильной группы в молекулу бензола активирует ее в реакциях электрофильного замещения.
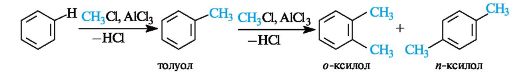
В реакциях алкилирования помимо алкилгалогенидов могут быть использованы и другие источники карбокатионов - алкены и спирты (в кислой среде).
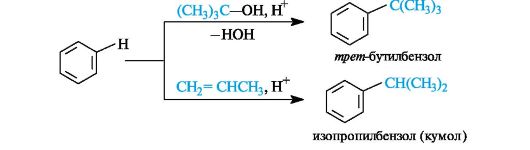
Галогенирование. Замещение свободным хлором или бромом в бензоле непосредственно не происходит, например, бензол не обесцвечивает бромную воду. Реакция проходит только в присутствии катализаторов, в частности FeCl3.
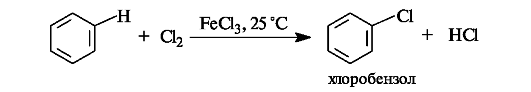
В качестве электрофила выступает либо комплекс галогена с FeCl3, в котором связь между атомами галогена сильно поляризована,
либо катион галогена, образовавшийся в результате диссоциации этого комплекса.

Сульфирование. Бензол сульфируют дымящей серной кислотой, содержащей избыток растворенного в ней оксида серы(VI).
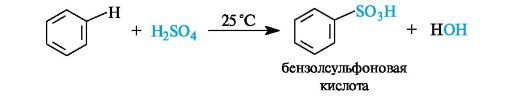
Сульфогруппа может легко удаляться из бензольного ядра, что используется в синтезе бактерицидных препаратов. Так, наиболее общий способ получения фенолов основан на сплавлении ароматических сульфоновых кислот со щелочами.
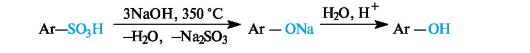
Реакции замещения в производных бензола. При взаимодействии бензола с электрофилом атакуется любой из шести равноценных атомов углерода ароматического кольца, что всегда приводит к единственному монозамещенному продукту. В случае монозамещенного бензола возможно образование трех изомеров - продуктов орто-, мета- и пара-замещения. Соотношение между ними, а также реакционная способность монозамещенного бензола по сравнению с незамещенным определяются природой имеющегося заместителя
Примеры реакций электрофильного замещения.
Нитрование
Нитрование, как правило, проводят смесью концентрированных азотной и серной кислот, так называемойнитрующей смесью. На первой стадии реакции происходит образование электрофильного агента - иона нитрония +NO2:
Затем катион нитрония вступает в реакцию с ароматическим субстратом, например бензолом:
Галогенирование
В отличие от нитрования, при галогенировании атака ароматического субстрата может осуществляться различными электрофилами. Свободные галогены, например, Cl2 и Br2, могут легко атаковать активированное ароматическое ядро (например, фенола), но не способны реагировать с бензолом и алкилбензолами. Для поляризации атакующей молекулы галогена необходим катализ кислотами Льюиса, такими как AlCl3, FeBr3, и т.п.; при этом в молекуле галогена появляется так называемый "электрофильный конец" (энергия же, требующаяся для образования катиона Наl+ существенно выше). Тем самым электрофильное замещение существенно облегчается:
Сульфирование
Арены взаимодействуют с концентрированной серной кислотой или олеумом (раствор SO3 в серной кислоте) с образованием аренсульфокислот:
ArH + H2SO4 ® ArSO3H + H2O
Электрофильной частицей является SO3. Атаку ароматического субстрата осуществляет атом серы, поскольку он сильно положительно поляризован, то есть электронодефицитен:
Сульфирование является обратимым процессом. Сульфогруппа может удаляться из ароматического ядра, что широко используется в органическом синтезе.
Электрофильное замещение в конденсированных ароматических углеводородах.
Конденсированные ароматические углеводородв обладают большей реакционной способностью, чем бензол, так как энергия сопряжения, приходящаяся на одно ароматическое кольцо в них меньше, чем в бензоле.
Для замещении в нафталине возможно образование двух изомерных продуктов при атаке электрофила в a - или в b -положение. Атомы водорода в a -положении обладают более высокой реакционной способностью и, если реакция протекает в условиях кинетического контроля (хлорирование, нитрование), то образуется a -изомер:
Сульфирование нафталина концентрированной серной кислотой при 80оС приводит к a-изомеру, который образуется с большей скоростью (кинетический контроль), а при 160оС – к термодинамически более стабильному b-изомеру (термодинамический контроль).
Еще более высокой реакционной способностью по сравнению с бензолом обладает антрацен. При этом во всех случаях атака электрофильных реагентов происходит по центральному ядру, а периферийные бензольные ядра сохраняются:

