Вопрос 1 Биохимия и медицина. Вклад биохимических исследований в диагностику и лечение заболеваний. Элементарный состав и основные классы природных биомолекул организма человека.
Быстрое развитие науки играет с нами грустную шутку. Новые знания и открытия появляются так быстро, что внедрение их в практику человеческой деятельности начинает сильно запаздывать. Порой у этой задержки причины даже не технологические, а сугубо ментальные. Причины кроются в стереотипах. А еще в том, что скорость изменения программ обучения отстает от скорости внедрения технологий в практику. В медицине, для которой характерен и естественнен повышенный консерватизм, это порой особенно заметно.
Когда студенты медицинских вузов изучают на 2-м или 3-м году обучения биохимию, приходится сталкиваться со своеобразной противоречивой ситуацией. Нередко изучение биохимии (как и многих других "теоретических" дисциплин) воспринимается как некоторая обязаловка, как нечто необходимое, но трудное и неочевидно полезное. Почему так? Ведь это происходит вопреки тому, что без понимания биохимической логики современная медицина уже не способна существовать.
Частичное объяснение может дать такой штрих: нередки случаи, когда уже на более старших курсах студенты возвращаются к изучению биохимии (патобиохимии) уже самостоятельно. Получается, для понимания важности биохимии студент-медик должен столкнуться с клиническими знаниями? Весьма на то похоже. (Впрочем, подобное "прозрение" затрагивает и ту же химию, физиологию и т.д.)
Есть ли сегодня сомнения, что любые физиологические процессы имеют свою химическую основу на молекулярном уровне? Химические реакции, протекающие в организме, их сочетание и особенности взаимосвязей между ними определяеют существование тела человека. Но - более того - сегодня уже можно говорить, что и поведение человека в целом, его психические реакции не могут быть независимыми от строения индивидуального генома и особенностей обмена веществ у одного отдельного взятого человека.
Какие же возможности дает понимание молекулярных причин и механизмов развития заболеваний?
1. Однозначно или с высокой вероятностью подтверждать диагноз заболевания и выявлять патологии еще до появления видимых признаков болезни (в том числе речь идет о пренатальной диагностике - обнаружении заболевания у еще не рожденного плода).
2. Разрабатывать способы лечения и непосредственно лечить пациента, воздействуя на причину его страданий, а не путем только устранения симптомов заболевания.
3. Целенаправленно создавать новые, более эффективные лекарства и нефармакологические методы лечения.
4. Предсказывать вероятность развития той или иной болезни у конкретного человека в будущем.
5. Принципиально изменить принципы профилактической медицины - на основе оценки степени персонального риска развития заболеваний можно будет перейти от "среднестатистических" программ предупреждения ряда заболеваний к профилактике персонифицированной.
6. Оценивать (обобщенно, так сказать вероятностно) наличие каких сочетанных патологий у пациента способно модифицировать эффект лечения основного заболевания и может повлиять.
7. Персонально оценивать вероятную эффективность лечения пациента с использованием лабораторных тестов (в идеале - еще до начала лечения) и осуществлять индивидальный подбор дозы используемых лекарственных препаратов.
Вот преимущества, которые уже дает и может дать в будущем развитие фундаментальной биохимии и молекулярной биологии.
Биомолекулы – органические соединения, входящие в состав организмов, образующие клеточные структуры и участвующие в биохимических реакциях обмена веществ.
Функции биомолекул в живых организмах.
а) участие в реакциях обмена веществ в роли промежуточных продуктов (метаболитов). Например, аминокислоты, моносахариды, жирные кислоты и др.
б) участие в образовании сложных молекул (белков, нуклеиновых кислот, липидов, полисахаридов) или биологических структур (мембран, рибосом, ядерного хроматина и др.).
в) участие в регуляции биохимических процессов и функций отдельных клеток и организма в целом (витамины, гормоны, циклические нуклеотиды цАМФ, цГМФ и др.).
Основные классы биомолекул:
Белки и аминокислоты. Белки – протеины (protos первый, значимый), важнейший класс биомолекул, с наличием которых связывают существование жизни в условиях Земли. Белки являются молекулами, в состав которых входят 20 аминокислот. Совокупность белков в организме составляет его протеом.
Нуклеиновые кислоты и нуклеотиды. Дезоксирибонуклеиновая (ДНК) и рибонуклеиновая (РНК) кислоты – биополимеры, состоящие из пуриновых и пиримидиновых нуклеотидов. Они являются носителями генетической информации у всех живых организмов. Последовательность мононуклеотидов в составе нуклеиновых кислот детерминирует (кодирует) последовательность аминокислотных остатков в белках. Последовательность из трех нуклеотидов (триплет или кодон) в молекуле ДНК соответствует одной из 20 аминокислот. Таким образом, генетический код определяет порядок включения аминокислот в полипептидную цепь в процессе синтеза белка на рибосомах. Совокупность генов в организме составляет его геном.
Нуклеиновые кислоты впервые обнаружил в ядрах клеток Фридрих Мишер (1869 г.). Приблизительно через 100 лет (в 1953 г) Д.Уотсон и Ф.Крик сделали фундаментальное открытие, описав структуру ДНК. Это позволяло раскрыть главную загадку жизни – обеспечение наследственности путем копирования наследственных признаков. Изучение функций РНК позволили сформулировать основную догму молекулярной биологии, которая определяет направление передачи генетической информации у всех живых организмов:
ДНК → РНК → Белок
Совокупность информационных РНК в организме составляет его транскриптом.
Углеводы – молекулы, состоящие из моносахаридов и их производных (дисахаридов, гомои гетерополисахаридов). В животных организмах моносахариды и гомополисахарид гликоген в основном исполняют энергетические функции, а гетерополисахариды принимают участие в образовании мембран, гликокаликса, соединительной ткани и т.д..
Липиды – молекулы, особенностью которых является гидрофобная природа. Липиды выступают как энергетический материал (нейтральные жиры), являются структурными компонентами мембран (фосфолипиды, гликолипиды) и биорегуляторами (стероидные гормоны, эйкозаноиды, жирорастворимые витамины).
Витамины – соединения с различным химическим строением, не синтезирующиеся в животных организмах, но необходимые для их жизнедеятельности. Они должны постоянно поступать в организм с продуктами питания, обеспечивая нормальное течение метаболических процессов, так как являются компонентами ферментных систем.
Гормоны и медиаторы – молекулы, передающие химические сигналы. Благодаря регуляторному действию гормонов и медиаторов нервной системы происходит интеграция отдельных анатомо-физиологических систем в целостный многоклеточный организм.
Кроме того в организме имеются свободные аминокислоты, азотистые соединения, нуклеотиды, низкомолекулярные моно-, дии трикарбоновые кислоты, спирты, амины, являющиеся промежуточными продуктами метаболизма (метаболитами или интермедиатами). Совокупность всех метаболитов в организме составляет его метаболом.
Клетка – структурная, функциональная и генетическая единица живого организма. Все клетки способны к размножению путем деления, передавая потомкам свои биологические признаки. Клетки делятся на прокариотические (безядерные) и эукариотические (ядерные). Они отличаются по химическому составу и обмену веществ.
Клеточные компоненты постоянно обновляются. Для тела человека период полуобновления белков (Т1/2) составляет в среднем 12 недель, белков печени меньше – 2 недели, белков мышц 27 недель, белков костной ткани – много месяцев.
Происхождение биомолекул. Фундаментальной проблемой биохимии является возникновение жизни на Земле. Согласно существующим представлениям, образование биомолекул и первых примитивных живых клеток происходило на Земле под действием физических факторов атмосферы приблизительно 3 млрд. лет тому назад
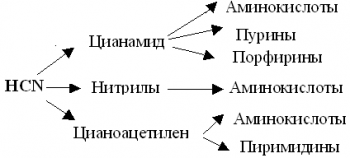
Стенли Миллер (1953г.), обнаружил возможность образования аминокислот при действии электрических разрядов на смесь метана, аммиака, водорода и водяного пара. В этих реакциях синтеза центральное место занимает цианистый водород – НСN, который может образовываться в реакции: CH4 + NH3 → HCN + 3H2
В дальнейшем цианистый водород превращается в цианамид, нитрит и цианоацетилен – предшественники аминокислот, пуринов, пиримидинов, порфиринов.
Пока необъяснимой проблемой в вопросе происхождения жизни является происхождение первичных информационных молекул
Источник: http://murzim.ru/nauka/biohimija/24506-biomolekuly.html
Вопрос 2 Ферменты гликолиза
Ферменты, осуществляющие отдельные этапы гликолиза:
1. Гексокиназа КФ2.7.1.1 (или глюкокиназа КФ2.7.1.2)
2. Гликогенфосфорилаза КФ2.4.1.1
3. Фосфоглюкомутаза КФ2.7.5.1
4. Глюкозофосфатизомераза КФ5.3.1.9
5. Фосфофруктокиназа КФ2.7.1.11
6. Фруктозобисфосфатальдолаза КФ4.1.2.13
7. Триозофосфатизомераза КФ5.3.1.1
8, 9. Глицеральдегидфосфатдегидрогеназа КФ1.2.1.12
10. Фосфоглицераткиназа КФ2.7.2.3
11. Фосфоглицеромутаза КФ2.7.5.3
12. Енолаза КФ4.2.1.11
13. Пируваткиназа КФ2.7.1.40
14. Лактатдегидрогеназа КФ1.1.1.27
Гликолиз начинается с образования фосфорных производных сахаров, что способствует превращению циклической формы субстрата в ациклическую, более реакционноспособную. Одной из реакций, регулирующих скорость гликолиза, является реакция 2, катализируемая ферментом фосфорилазой. Центральная регуляторная роль в гликолизе принадлежит ферменту фосфофруктокиназе (реакция 5), активность которой тормозится АТФ и цитратом, но стимулируется продуктами ее распада. Центральным звеном гликолиза является гликолитическая оксидоредукция (реакции 8–10), представляющая собой окислительно-восстановительный процесс, протекающий с окислением 3-фосфоглицеринового альдегида до 3-фосфоглицериновой кислоты и восстановлением кофермента никотинамидадениндинуклеотида (НАД). Эти превращения осуществляет дегидрогеназа 3-фосфоглицеринового альдегида (ДФГА) при участии фосфоглицераткиназы. Это – единственный окислительный этап в гликолизе, но и он не требует свободного кислорода, необходимо лишь присутствие НАД+, который при этом восстанавливается до НАД-Н2.
В результате оксидоредукции (окислительно-восстановительный процесс) высвобождается энергия, аккумулирующаяся (в виде богатого энергией соединения АТФ) в процессе субстратного фосфорилирования. Второй реакцией, обеспечивающей образование АТФ, является реакция 13 – образование пировиноградной кислоты. В анаэробных условиях гликолиз кончается образованием молочной кислоты (реакция 14) под действием лактатдегидрогеназы и с участием восстановленного НАД, который при этом окисляется до НАД (НАД-Н2) и вновь может быть использован на окислительном этапе. В аэробных условиях пировиноградная кислота окисляется в митохондриях в ходе цикла Кребса.
Т.о., при расщеплении 1 молекулы глюкозы образуются 2 молекулы молочной кислоты и 4 молекулы АТФ. В то же время на первых стадиях гликолиза (см. реакции 1, 5) затрачиваются 2 молекулы АТФ на 1 молекулу глюкозы. В процессе гликогенолиза образуется 3 молекулы АТФ, т.к. не нужно тратить АТФ для получения глюкозо-6-фосфата. Первые девять реакций гликолиза представляют собой его эндергоническую (с поглощением энергии) фазу, а последние реакции – экзергоническую (с выделением энергии) фазу. В процессе гликолиза выделяется только около 7% теоретической энергии, которая может быть получена при полном окислении глюкозы (до СО2 и Н2О). Однако общая эффективность накопления энергии в форме АТФ составляет 35–40%, а в практических условиях клетки может быть и выше.
Глицеральдегидфосфатдегидрогеназа и лактатдегидрогеназа внутренне сопряжены (один требует НАД+, другой образует НАД+), что обеспечивает круговорот этого кофермента. В этом, возможно, заключается основное биохимическое значение терминальной дегидрогеназы.
Все реакции гликолиза обратимы, кроме 1, 5 и 13. Однако можно получить глюкозу (реакция 1) или фруктозомонофосфат (реакция 5) из их фосфорных производных при гидролитическом отщеплении фосфорной кислоты в присутствии соответствующих ферментов; реакция 13 практически необратима, по-видимому, вследствие высокой энергии гидролиза фосфорной группировки (около 13 ккал/моль). Поэтому образование глюкозы из продуктов гликолиза идет другим путем.
В присутствии O2 скорость гликолиза снижается (эффект Пастера). Есть примеры подавления гликолизом тканевого дыхания (эффект Кребтри) в некоторых интенсивно гликолизирующих тканях. Механизмы взаимоотношений анаэробных и аэробных окислительных процессов до конца не изучены. Одновременное регулирование процессов гликолиза и гликогенеза однозначно определяет поток углерода по каждому из этих путей в зависимости от нужд организма. Контроль осуществляется на двух уровнях – гормональном (у высших животных через регуляторные каскады с участием вторичных посредников) и метаболическом (у всех организмов).